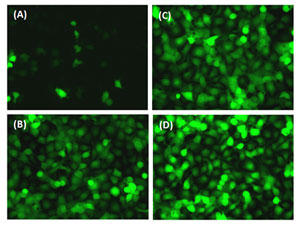
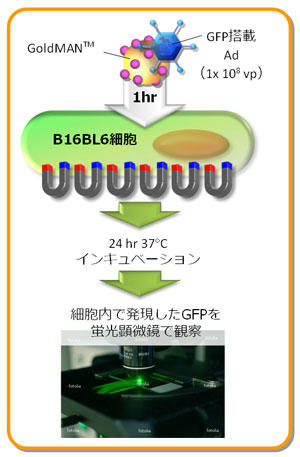
図3、Ad/GoldMAN™複合体のB16BL6 CAR (-)細胞への遺伝子導入(Fig.1使用)
Ad/GoldMAN™複合体による遺伝子導入効率は、Ad-EGFPの1.0 x 108 vpを使用して評価した。B16BL6細胞のEGFP発現は、蛍光顕微鏡によって観察した。
(A) 磁力なしの条件で、Ad-EGFP/GoldMAN™複合体をトランスフェクションした。
(B)-(D) 磁力をかける時間を(B)15分、(C)30分、(D)60分でAd-EGFP/GoldMAN™をトランスフェクションした。
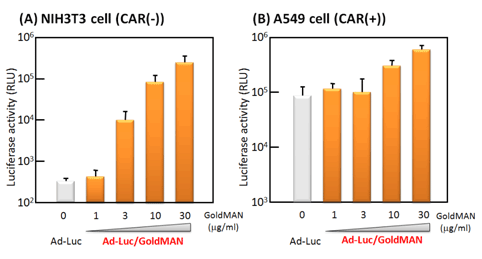
図4、Ad/GoldMAN™複合体のNIH3T3細胞とA549細胞への遺伝子導入(Fig.2使用)
Ad/GoldMAN™複合体による遺伝子導入効率は、Ad-Luc (Luciferase expressing Ad)の1.0 x 108 vp を使用して評価した。(A)NIH3T3 CAR(-)細胞、(B)A549 CAR(+)細胞。
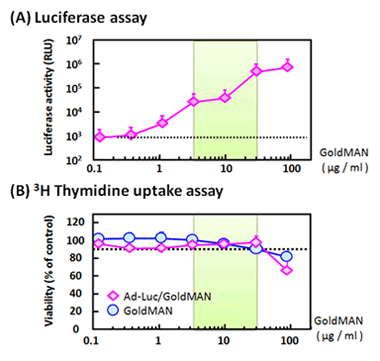
図5、GoldMAN™による形質導入の効率と安全性(Fig.3使用)
(A) ルシフェラーゼアッセイ
Ad-Luc (Luciferase expressing Ad)の1.0 x 108 vpを使用して、Ad/GoldMAN™の遺伝子発現を定量した。連続的に希釈したGoldMAN™をAd-Lucと混合し、ルシフェラーゼ発現(RLU)を市販のアッセイシステムによって測定した。緑色の範囲は、形質導入の効率と安全性における最適条件を表す。
(B) 3H-チミジン取り込みアッセイ
Ad/GoldMANの細胞毒性を[3H]-チミジンの取り込みによって評価した。緑色の範囲は、形質導入の効率と安全性における最適条件を表す。























 このページを印刷する
このページを印刷する












 中身を見る
中身を見る 中身を見る
中身を見る 中身を見る
中身を見る
 中身を見る
中身を見る