本商品は、生細胞中の一酸化窒素(NO)を蛍光で検出するキットです。

一酸化窒素(NO)は、多くの生理学的・病理学的プロセスに関与する重要な生物学的レギュレーターです。NO産生に変化が生じると、免疫系や血管系、神経変性、炎症性など様々な疾患に影響を及ぼします。NOはフリーラジカルのため、生体内では迅速に酸化され、比較的低濃度で存在します。そのため、生物学的システムにおけるNOの役割を検出および理解することは容易ではありません。
本商品では、生細胞の細胞内NOレベルを高感度にモニターできます。Nitrixyte™ プローブは DAF-2 の優れた代替として、細胞内のフリーNOの検出に使用されます。Nitrixyte™ はDAF-2と比較して光安定性が高く、細胞透過性が強化されています。
AAT Bioquest社では、Cy3® や TRITC と類似のスペクトル特性を有する Nitrixyte™ Orange(Ex/Em 488/590 nm)、Texas Red® と類似のスペクトル特性を有する Nitrixyte™ Red(Ex/Em 630/660 nm)、近赤外蛍光スペクトルの Nitrixyte™ NIR(Ex/Em 650/680 nm)を使用したキットをご用意しています。
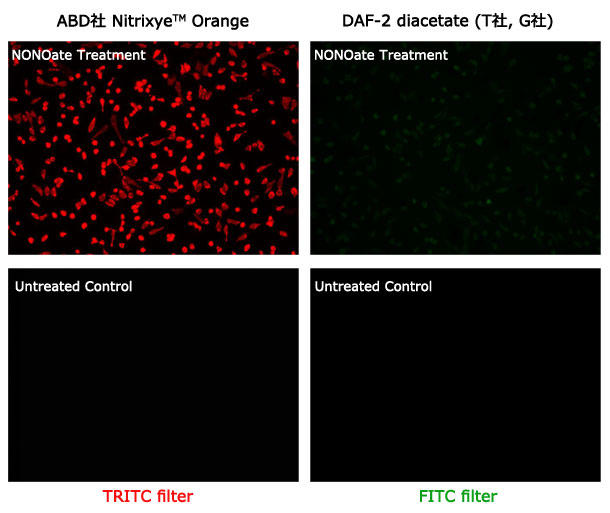
図1. 外因性一酸化窒素(NO)の蛍光イメージング
HeLa細胞で NONOate(NOドナー)処理における外因性 NO の蛍光イメージングを行った。細胞は AAT Bioquest (ABD) 社のNitrixyte™ Orange (左) もしくは DAF-2 diacetate (右)を同濃度で 30分間インキュベートした後、1 mM DEA NONOateで37℃ 30分間処理した。蛍光シグナルは蛍光顕微鏡のTRITC(左)とFITC(右)のフィルターでそれぞれ検出した。
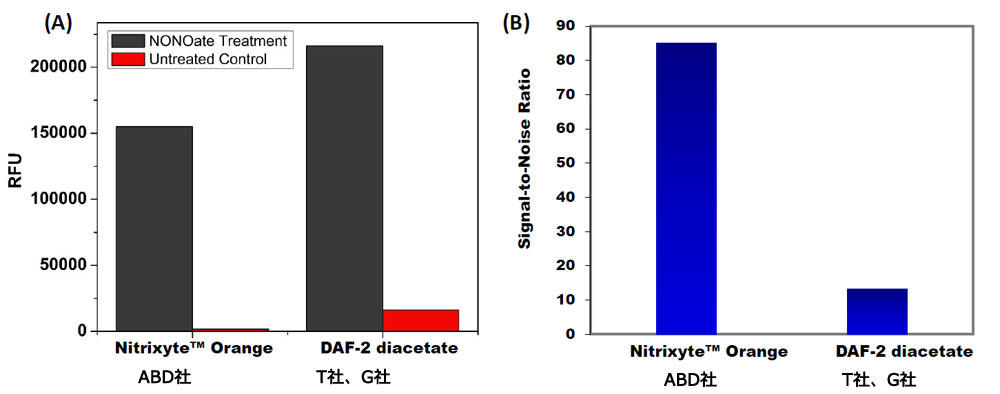
図2. 外因性一酸化窒素(NO)のマイクロプレートリーダーによる測定
HeLa細胞における NONOate(NOドナー)処理における外因性NO をマイクロプレートリーダーで測定した。細胞はABD社のNitrixyte™ Orange (左) もしくはDAF-2 diacetate (右)を同濃度で30分間インキュベートした後、37℃ 30分間 1mM DEA NONOate 処理した。蛍光シグナルは Ex/Em = 540/590 nmもしくは Ex/Em = 490/530 nm でそれぞれ測定した。
(A)で示したNONOate処理サンプルのRFUを対応する非処理コントロールのRFUで割った値を(B)シグナル-ノイズ比として示した。
DAF-2 diacetateに比べ、Nitrixyte™ Orangeは優位に高いシグナル-ノイズ比を示した。
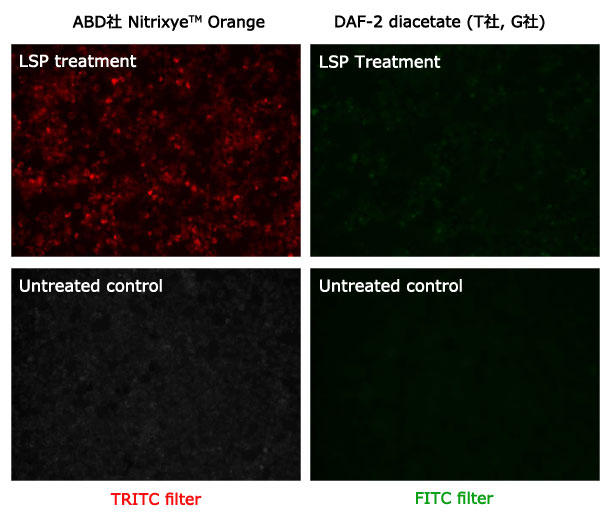
図3. 内因性一酸化窒素(NO)の蛍光イメージング
RAW 264.7 マクロファージにおける内因性NO の蛍光イメージングを行った。細胞はABD社の Nitrixyte™ Orange (左) もしくは DAF-2 diacetate (右)を同濃度で 30分間インキュベートした後、20 µg/mL リポポリサッカライド(LPS)と1 mM L-アルギニン(L-Arg)で 37℃ 16時間処理した。蛍光シグナルは蛍光顕微鏡の TRITC(左)とFITC(右)のフィルターでそれぞれ検出した。
| 細胞の用意 |
|
| ワーキング溶液の調製 |
|
| NOアッセイ |
|
図4. Jurkat細胞を用いたNOの検出
一酸化窒素供与体であるDEA NONOateで処理したもの(赤色)とDEA NONOateで未処理のもの(青色)のシグナルをフローサイトメーターで検出した。
(上段左)品番:16351 (上段右)品番:16356 (下段左)品番:16360
図5. DEA/NONOate処理(NOドナー)したCHO-K1細胞、HeLa細胞のNO検出(品番:16350)
各細胞をNitrixyte™ Orangeワーキング溶液で37℃、30分間インキュベートした後、染色を停止するためワーキング溶液を除去した。さらに 10 mM HEPES(pH=6.2)を持つHBSSに 1 mM DEA/NONOate を含むもの、含まないもので処理し、37℃、30分間インキュベートした。各ウェルの溶液を除去後アッセイバッファーII を添加し、蛍光シグナルを測定 (FlexStation (Molevular Device)、Ex/Em = 540/590 nm (cut off = 570 nm)、bottom read mode)。
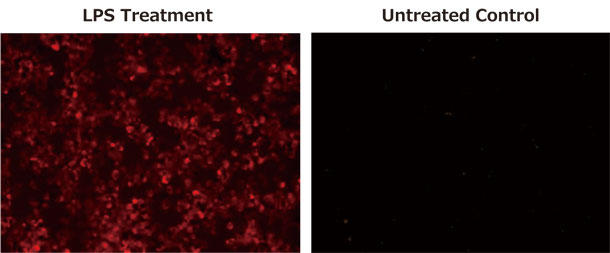
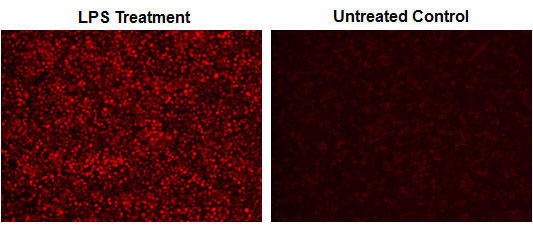
図6. RAW 264.7 マクロファージ細胞のNO検出
培地に Nitrixyte™ プローブ試薬を加え、かつ20 µg/mLのLPSと1 mMのL-アルギニン(L-Arg)を含む培地と含まない培地に分け、37℃で16時間インキュベートした。各ウェル内の溶液を取り除き、アッセイバッファーII(Component C)を加え、蛍光シグナルを測定。
(上段)Nitrixyte™ Orange (品番:16350)、(下段)Nitrixyte™ NIR(品番:16359)
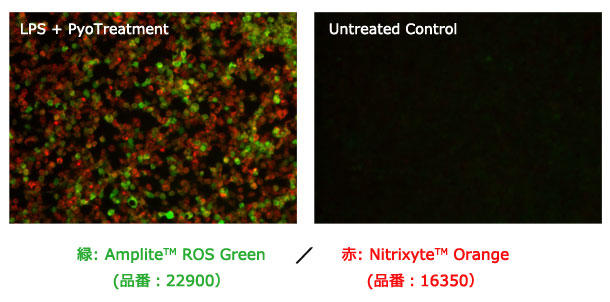
図7. 細胞内一酸化窒素 (NO) とトータルROS の同時蛍光イメージング
RAW264.7マクロファージの細胞内NOとトータルROSの蛍光イメージングを同時に行った。 AAT社のNitrixyteTM Orange (品番:16350)とAmpliteTM ROS Green (品番:22900)で共染色した後、 20ug/mL リポポリサッカライド(LPS)、1 mM L-アルギニン(L-Arg)、50 uM Pyocyanin (Pyo)で 37℃ 16時間処理した。蛍光シグナルは蛍光顕微鏡のTRITC(赤 NitrixyteTM Orange )とFITC(緑 AmpliteTM ROS Green )のフィルターでそれぞれ検出した
Nitrixyte™ NIR
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Cell MeterTM Fluorimetric Intracellular Nitric Oxide (NO) Activity Assay Kit *NIR Fluorescence Optimized for Flow Cytometry* |
ABD | 16360 | 100 TEST |
¥84,000 |
Cell MeterTM Fluorimetric Intracellular Nitric Oxide (NO) Activity Assay Kit *NIR Fluorescence Optimized for Microplate Reader* |
ABD | 16359 | 200 TEST |
¥84,000 |
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Cell MeterTM Fluorimetric Intracellular Nitric Oxide (NO) Activity Assay Kit *Orange Fluorescence Optimized for Flow Cytometry* |
ABD | 16351 | 1 KIT [100 Tests] |
¥84,000 |
Cell MeterTM Fluorimetric Intracellular Nitric Oxide (NO) Activity Assay Kit *Orange Fluorescence Optimized for Microplate Reader* |
ABD | 16350 | 1 KIT [200 Tests] |
¥84,000 |
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Cell MeterTM Fluorimetric Intracellular Nitric Oxide (NO) Activity Assay Kit *Red Fluorescence Optimized for Flow Cytometry* |
ABD | 16356 | 100 TEST |
¥84,000 |
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について
© COSMO BIO