免疫組織染色(IHC)は、微細構造を保持したそのままの組織中のタンパク質、別の言い方をすると、「現実」を可視化することができます。「現実」を可視化する利点の一つは、正常組織と病変組織とを比較できることであり、科学者と病理学者のどちらにとっても非常に貴重な手法であると言えます。IHCのプロトコールは簡単ですが、標的タンパク質に抗体が特異的に結合し、最適に可視化するためには、最初に多くのステップで最適化を行う必要があります。本稿では、各ステップのヒントをいくつかご紹介し、少し調整が必要となる点をご説明していきます。
技術情報
1. 組織の調製
組織サンプルは、凍結または固定することができます。切片を凍結すると、通常は標的抗原の立体構造が維持されるため、優れた抗体結合が可能ですが、組織内に小さな氷晶が形成される可能性があり[1, 2]、長期保存には適さない場合があります。組織の固定や包埋は、スライドをもう少し長く保存したい場合に良い方法です。組織の固定・包埋法で最も一般的なのは、ホルマリン固定パラフィン包埋(FFPE)です。(FFPE生検組織は、室温で無期限に保存できることから、医学史研究の重要な資源となります!)
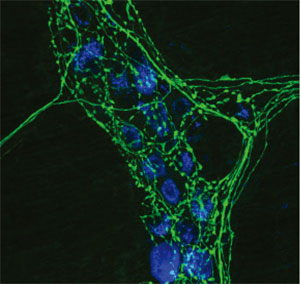
共焦点レーザー走査型顕微鏡によるIHC染色画像。青色: UV領域での節後ニューロンの自家蛍光。
出典: Wikimedia commons
2. 組織の調製: その他に試すこと
組織切片を染色する前に、氷冷した 50:50 メタノール‐アセトン(MeAc)または 4% パラホルムアルデヒド(PFA)で固定すると、抗体の結合が増強される場合があります。例えば、MeAc は細胞質タンパク質を溶解することから、膜結合タンパク質がより見やすくなります。
3. 抗原の賦活化
ホルムアルデヒド固定は、組織内のタンパク質を架橋し、組織の形態を維持することができますが、抗体が認識するエピトープの変性が起こります[3]。そのため、通常は FFPE 切片を染色する前に、抗原の賦活化を行い、覆われた(または変性した)標的エピトープを再び露出させます。抗原の賦活化は、加熱または酵素処理によって行い[4]、温度、pH、時間などの素因が影響します。初めて使用する抗体と組織の場合には、抗原賦活化法を一通り試して、非特異的なバックグラウンドを抑制する最適な染色方法を決定することをお奨めします[5]。まず始めに、電子レンジを用いて、pH 6.0 のクエン酸バッファー中で沸騰させる方法を試してみてください。凍結切片の場合は、抗原賦活化は不要ですが、染色する前に切片を少なくとも1時間は風乾する必要があります。FFPE切片は、抗原賦活化や染色を行う前に、キシレンとアルコールで脱パラフィンを行う必要があります。切片は、脱パラフィンを行った後、アルコール濃度を段階的に下げてから水に浸すことで再水和します。(次のヒントに続きます)
4. サンプルの取り扱い
切片を脱パラフィン・再水和した後は、完全に乾かさないようにすることが重要です! そのため、インキュベーション中の切片を入れておく、IHC染色専用の容器(多数市販されており、組織切片の湿度を保つことができます)を使用してください。
Top tip
PAPペン(サンプルの周囲にサークルを描くと、薄いフィルム状の疎水性の囲いを作ることができるマーキングペン)を使用すると、透過処理を行った切片の近くに溶液を留めることができます。PAPペンは必須ではありませんが、使用すると便利です。(PAPペンは、透過処理や MeAc 固定を行う前には使用しないでください。Triton や MeAc に溶解するため、組織に付着する場合があります。)
5. 透過処理
ほとんどのタンパク質は、プロトコールに透過処理ステップを追加することをお奨めします。膜貫通タンパク質は、エピトープが細胞外領域に存在するため、透過処理が不要な場合があります。透過処理には、界面活性剤(例: 0.1% Triton-X100 in PBS)とのインキュベーションが含まれます。界面活性剤は、ホルムアルデヒド固定で形成されたタンパク質架橋の一部を壊すことから、抗体の正しいエピトープへの結合を促進し[1]、非特異的な疎水性相互作用を低減します。
Top tip染色がうまくいかない場合は、すべての溶液に界面活性剤(Triton など)を低濃度で添加してみてください(特にFFPE切片を染色する場合)。
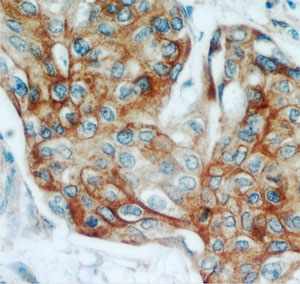
Proteintech社の KRT13 ポリクローナル抗体(品番: 10164-2-AP)を用いた、ホルマリン固定パラフィン包埋した子宮頸癌の免疫組織染色(40×)。一般的に、ポリクローナル抗体は同じタンパク質上の数種類のエピトープを認識するため、明るいIHCシグナルが得られる。
出典: Proteintech社 データシート(品番: 10164-2-AP)
6. ブロッキング
ブロッキング溶液は、組織内の非特異的な部位に結合して[1]、一次/二次抗体が組織成分に非特異的に結合することを防ぎます。ウシ血清アルブミン(BSA)や二次抗体の宿主の血清などの「反応に影響しないタンパク質溶液」で、切片をインキュベートします。通常は、3% BSA で 20-30 分間インキュベートすることから始めます。また、Proteintech社では通常 3% BSA を使用していますが、5-10% ヤギ血清を使用することもできます(二次抗体のホスト動物種(免疫動物)がヤギの場合)。
7. 一次抗体の選択
一次抗体は、目的のタンパク質の発現レベルや、共局在の解析に使用する他の抗体などを考慮して、選択する必要があります。後者の場合は、それぞれ別の標識をした、種の異なる二次抗体を使用することで識別します。また、必要に応じてモノクローナルとポリクローナルから選択します。モノクローナル抗体を使用すると特異性の高いシグナルが、ポリクローナル抗体を使用すると(目的のタンパク質の発現レベルが低い場合には特に)明るいシグナルが得られます。
Box 1: コントロール
宿主血清中の他の抗体に対して、交差反応したり、非特異的に結合したりする可能性が考えられます。このような問題が起こることを防ぐために、プロテインA/G精製、アフィニティー精製、吸着処理などの精製技術を利用します。Proteintech社の抗体製品は全て、標的抗原でアフィニティー精製されていますが、もし、一次抗体の結合特異性を確認するためにコントロールを用いる場合は、下記をご参照ください。
理想的なコントロールとなるのは、目的のタンパク質を含まない組織です。例えば、ノックアウトマウスの組織や、目的のタンパク質が(siRNA などで)ノックダウンされた細胞などを使用します。
抗体が、正しいサイズのタンパク質を検出することを確認するためには、ウェスタンブロットを行います。ウェスタンブロットで複数のバンドが検出される場合、抗体の非特異的な結合が示唆されます。
抗体の特異性は、一次抗体と抗原ペプチドをプレインキュベーションすることで確認できます(吸収試験)。抗体がアフィニティー精製されている場合は、タンパク質の精製に特異的なペプチド配列を使用しているため、このステップは必要ありません[6]。
カスタム作製した抗体の場合は、作製過程の様々なステップの血清を用いてウェスタンブロットを行い、目的のタンパク質を示すバンドが正しい画分に検出されるかどうかを確認してください。
8. 抗体の希釈
通常、抗体の希釈率はデータシートに記載されていますが、記載がない場合は、まず 1:50 - 1:300 で希釈し、最適化することをお奨めします。新しい抗体を使用する際には、様々な希釈率を試してみてください。一次抗体をブロッキング溶液(例: 3% BSA in PBS)で希釈し、室温で1-2時間、または4℃で一晩インキュベートしてください。
9. 洗浄
PBSなどの洗浄溶液で一次抗体を洗い流してください。素早く洗浄した後、5分×3回洗浄すれば十分です。凍結切片は非常に壊れやすいため、溶液は切片の近くにゆっくり滴下してください(例: 1 mL ピペットなどを使用)。
Top tip洗浄バッファーをPBSではなく、TBS(Tris-buffered Saline)に変更してください。
Box 2: 検出
一次抗体の検出は、蛍光(例: FITC)、または、発色による検出が可能な酵素(例: HRP / horse-radish peroxidase)で標識された、一次抗体の宿主のイムノグロブリンに対する二次抗体を用いて行います。 検出を成功させるためのヒントをご紹介します。
バックグラウンド染色は実験間でばらつきがあるため、実験ごとに、一次抗体を省略したネガティブコントロールを用いることをお奨めします。
二次抗体をブロッキング溶液で希釈します。通常は、約 1:800 - 1:1000 で希釈します(希釈率は適宜調節します)。
蛍光免疫染色の場合
使用する蛍光色素が、お持ちの顕微鏡で検出できることを確認してください。二次抗体に標識した蛍光色素のスペクトルの重複、二次抗体間の交差反応、イメージングの際の蛍光漏れに注意することが重要です。
蛍光抗体を添加したら、退色を防ぐために、切片を暗所においてください。
インキュベーション後、封入剤を添加する前に、切片をPBSで数回洗浄し、カバーガラスを上から慎重に下ろしてください。
気泡が入らないように、静かにカバーガラスを下します。凍結切片の場合は特に注意し、組織が破壊されるのを防ぐために、カバーガラスを強く押さないようにしてください。
核を染色すると(例: DAPI などで)便利です。洗浄ステップの間に行うか、封入剤に入れます。
一次抗体を蛍光タグで直接標識することも可能です。時間が短縮でき、偽陽性シグナルが減少しますが、シグナルのレベルが低下します。低レベルのシグナルを増幅する方法には、アビジン‐ビオチン複合体(ABC)、標識ストレプトアビジン‐ビオチン法(LSAB)などがあります。
10. 最適化の出発点
IHCのプロトコールには、最適化を要するステップが多くありますが、心配する必要はありません。IHC実験を始めるには、まず下記のステップから最適化を始めてください。
- FFPE切片の抗原賦活化
- 一次抗体の希釈
- ブロッキング溶液
◆◇【春の特典キャンペーン】日頃のご愛顧に感謝を込めて、商品発送時にギフトをお届けします ◇◆
◆◇【最短翌営業日にお届け!】約2万点の国内在庫をご用意しています ◇◆
◆◇【高感度なIHC染色に!ポリマー試薬も新登場】Multi-rAb(マルチ・ラブ)二次抗体 ◇◆
◆◇ トライアルサイズ抗体購入者限定!次回購入時に使えるお得なクーポン配布中 ◇◆
◆◇【ELISAキット¥80,000/96ウェル】プロテインテックの免疫アッセイキット ◇◆
◆◇ cGMPグレードも選べる!ヒト細胞由来のサイトカイン・増殖因子 ◇◆
◆◇ 次世代ツールのナノ抗体!アルパカ由来のVHH抗体(Nanobody®)製品 ◇◆
◆◇【アプリケーションノート公開中】実績急上昇!FlexAble抗体標識キット ◇◆
- Daneshtalab N, Doré JJ and Smeda JS, Troubleshooting tissue specificity and antibody selection: Procedures in immunohistochemical studies., J Pharmacol Toxicol Methods., 2010;61(2):127-35.
- Shi SR, Liu C, Pootrakul L et al., Evaluation of the value of frozen tissue section used as “gold standard” for immunohistochemistry., Am J Clin Pathol., 2008;129(3):358-66.
- Fox CH, Johnson FB, Whiting J et al., Formaldehyde fixation. J Histochem Cytochem., 1985;33:845–853.
- Yamashita S et al., Heat-induced antigen retrieval: mechanisms and application to histochemistry. Prog Histochem Cytochem., 2007;41:141-200.
- Shi SR, Cote RJ and Taylor CR, Antigen retrieval immunohistochemistry: past, present, and future. J Histochem Cytochem., 1997;45(3):327-43.
- Saper CB and Sawchenko PE, Magic peptides, magic antibodies: guidelines for appropriate controls for immunohistochemistry. J Comp Neurol., 2003;465:161–163.
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては
使用しないように、十分ご注意ください。