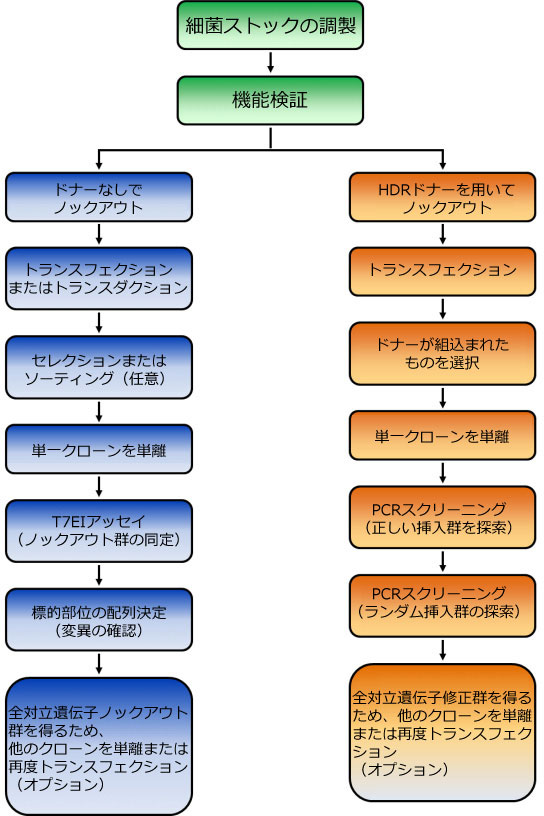
GeneCopoeiaپiGCPپjژذ‚جCRISPR-Cas9—p”ٌƒEƒCƒ‹ƒXگ«ƒvƒ‰ƒXƒ~ƒh‚حˆê”ت“I‚بژè–@‚إƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚إ‚«‚ـ‚·‚ھپA“ء’è‚جچ×–Eƒ^ƒCƒv‚ةچإ“K‰»‚¨‚و‚رŒںڈطچد‚جEndoFectin™ ƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“ژژ–ٍ‚à‚²’ٌ‹ں‚µ‚ؤ‚¢‚ـ‚·پBژg—pچ×–E‚ة“K‚µ‚½ژè–@پEژژ–ٍ‚ً‚²‘I‘ً‚‚¾‚³‚¢پBGeneCopoeiaپiGCPپjژذ‚جCRISPR-Cas9ƒŒƒ“ƒ`ƒEƒCƒ‹ƒXƒvƒ‰ƒXƒ~ƒh‚حپA‘و3گ¢‘م‚جƒŒƒ“ƒ`ƒEƒCƒ‹ƒXƒpƒbƒPپ[ƒWƒ“ƒOژژ–ٍ‚ة‘خ‰‚µ‚ؤ‚¨‚èپALentifect™ ƒŒƒ“ƒ`ƒEƒCƒ‹ƒXƒpƒbƒPپ[ƒWƒ“ƒOژژ–ٍ‚⃌ƒ“ƒ`ƒEƒCƒ‹ƒXƒpƒbƒPپ[ƒWƒ“ƒOƒTپ[ƒrƒX‚à‚²’ٌ‹ں‚µ‚ؤ‚¢‚ـ‚·پB”ٌƒEƒCƒ‹ƒXƒvƒ‰ƒXƒ~ƒh‚ئƒŒƒ“ƒ`ƒEƒCƒ‹ƒXƒvƒ‰ƒXƒ~ƒh‚ج‚¢‚¸‚ê‚àپAƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚âƒgƒ‰ƒ“ƒXƒ_ƒNƒVƒ‡ƒ“‚جچى‹ئچH’ِ‚ھٹب’P‚ة‚ب‚é‚و‚¤پA–ٍ•¨‘I‘ًƒ}پ[ƒJپ[‚ئŒuŒُƒŒƒ|پ[ƒ^پ[ˆâ“`ژq‚ً•غ—L‚µ‚ؤ‚¢‚ـ‚·پiگ}.3پjپB
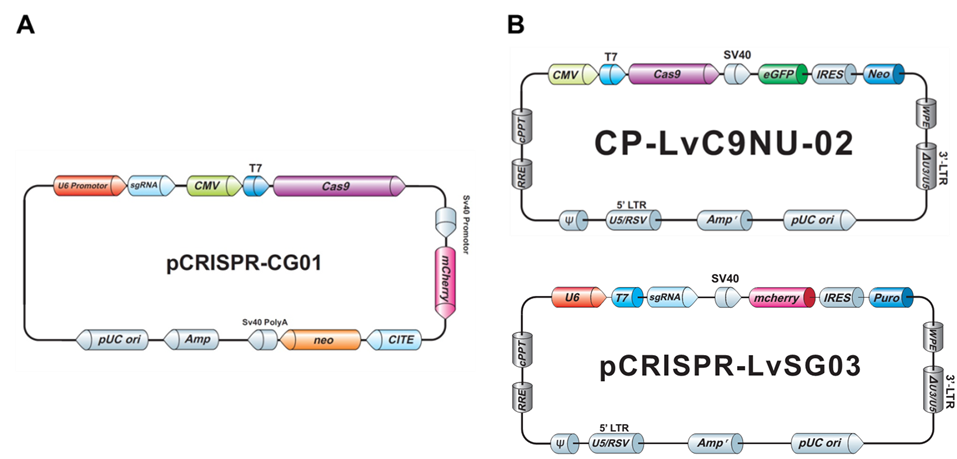
گ}.3پ@GeneCopoeiaپiGCPپjژذƒQƒmƒ€•زڈWƒvƒ‰ƒXƒ~ƒh‚جˆê—ل
A. CRISPR Cas9ƒkƒNƒŒƒAپ[ƒ[پA1ژي—ق‚جsgRNAپAG418‘I‘ً—pneoˆâ“`ژqپA‚¨‚و‚رŒuŒُƒŒƒ|پ[ƒ^پ[‚ئ‚µ‚ؤmCherry‚ًƒRپ[ƒh‚µ‚½”ٌƒEƒCƒ‹ƒXگ«‚جall-in-oneƒvƒ‰ƒXƒ~ƒh
B.ڈم•”پFneoˆâ“`ژq‚ئeGFP‚ًƒRپ[ƒh‚µ‚½CRISPR Cas9ƒkƒNƒŒƒAپ[ƒ[ƒxƒNƒ^پ[پiƒŒƒ“ƒ`ƒEƒCƒ‹ƒXƒvƒ‰ƒXƒ~ƒhپj
‰؛•”پFƒsƒ…پ[ƒچƒ}ƒCƒVƒ“‘I‘ً—ppuroˆâ“`ژq‚ئmCherry‚ًƒRپ[ƒh‚µ‚½CRISPR sgRNAƒvƒ‰ƒXƒ~ƒhپiƒŒƒ“ƒ`ƒEƒCƒ‹ƒXƒvƒ‰ƒXƒ~ƒhپj
ˆâ“`ٹw‚إ‚حپAپuƒNƒچپ[ƒ“’P—£پv‚ئ‚µ‚ؤ’m‚ç‚ê‚é‚و‚¤‚ةپAڈW’c‚©‚ç—£‚ꂽ•دˆظ‘ج‚ًگ¸گ»‚·‚邱‚ئ‚ھڈd—v‚إ‚·پBƒNƒچپ[ƒ“’P—£‚ًچs‚¤‚±‚ئ‚إپAŒ‹‰ت‚ج‰ًژك‚ًچ¬—گ‚³‚¹‚©‚ث‚ب‚¢چ×–E•ھ—ô‚âƒIƒtƒ^پ[ƒQƒbƒgچى—p‚ة‚و‚èگ¶‚¸‚éٹْ‘ز‚µ‚ب‚¢ڈCگ³‚ة‚و‚é‰e‹؟‚ًچإ’لŒہ‚ة—}‚¦‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پBƒXƒNƒٹپ[ƒjƒ“ƒO‚ًژn‚ك‚éچغ‚حپA‚ـ‚¸پA’PˆêƒRƒچƒjپ[‚ًŒ`گ¬‚إ‚«‚é‚و‚¤چ×–E‚ً”dژي‚µ‚ؤƒfƒBƒbƒVƒ…‚©‚çژو‚èڈo‚·‚©پA96ŒٹƒvƒŒپ[ƒg‚إ’iٹKٹَژك‚ً‚ئ‚è‚ـ‚·پB
ژہژ{‚·‚éƒXƒNƒٹپ[ƒjƒ“ƒO‚جƒ^ƒCƒv‚حپA‚ا‚ج‚و‚¤‚بƒQƒmƒ€•زڈW‚ًچs‚¤‚©‚ة‚و‚ء‚ؤˆظ‚ب‚è‚ـ‚·پB‚±‚±‚إ‚حپA3ژي—ق‚جˆê”ت“I‚بڈَ‹µ‚ًک_‹c‚µ‚ـ‚·پB
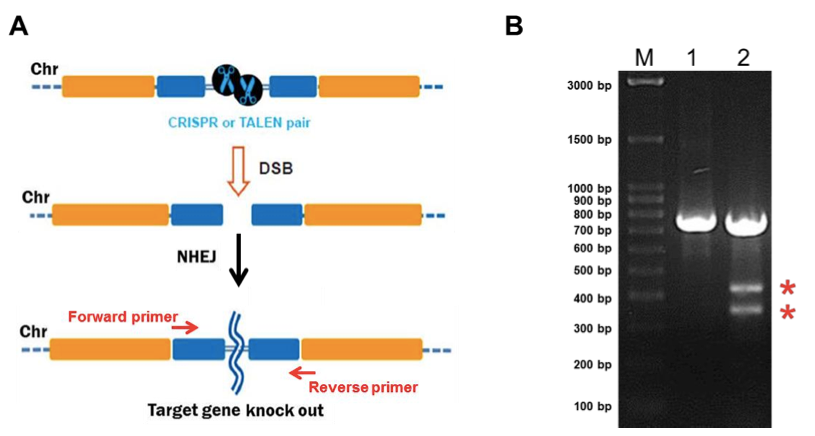
پ، NHEJپi”ٌ‘ٹ“¯––’[Œ‹چ‡پj‚ة‚و‚éƒmƒbƒNƒAƒEƒg
NHEJپi”ٌ‘ٹ“¯––’[Œ‹چ‡پj‰îچفگ«ƒmƒbƒNƒAƒEƒg‚ًگv‘¬‚ةƒXƒNƒٹپ[ƒjƒ“ƒO‚·‚é•û–@‚ئ‚µ‚ؤپA‹@”\Œںڈط‚جچ€‚ة‹Lچع‚ج‚ ‚éƒ~ƒXƒ}ƒbƒ`گط’fƒAƒbƒZƒC‚ھ‚ ‚è‚ـ‚·پBڈCگ³‚³‚ꂽƒNƒچپ[ƒ“‚ھ“¯’è‚إ‚«‚½Œم‚حپAPCRژY•¨‚ً—p‚¢‚ؤƒTƒ“ƒKپ[ƒVپ[ƒNƒGƒ“ƒX–@‚ة‚و‚é”z—ٌŒˆ’è‚ًچs‚¢پA•دˆظڈَ‘ش‚ً“¯’è‚·‚é•K—v‚ھ‚ ‚è‚ـ‚·پBGeneCopoeiaپiGCPپjژذ‚إ‚حپAƒNƒچپ[ƒ“ƒXƒNƒٹپ[ƒjƒ“ƒO‚ة—ک—p‚إ‚«‚éƒ~ƒXƒ}ƒbƒ`گط’fƒAƒbƒZƒCƒLƒbƒg‚ً‚²’ٌ‹ں‚µ‚ؤ‚¢‚ـ‚·پB
پ، ƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚ً—p‚¢‚½HRپiHDRپjƒAƒvƒٹƒPپ[ƒVƒ‡ƒ“
ˆê”ت‚ةپATALEN‚âCRISPR-Cas9‚ً‰î‚·‚é‘ٹ“¯گ«‘gٹ·‚¦•p“x‚حپANHEJپi”ٌ‘ٹ“¯––’[Œ‹چ‡پj‚ئ”ن‚ׂؤ‚©‚ب‚è’ل‚¢‚½‚كپAƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚ة‚و‚èڈCگ³‚³‚ꂽƒRƒچƒjپ[‚ً“¯’è‚·‚é‚ة‚ح‚و‚葽‚‚جƒRƒچƒjپ[‚ًƒXƒNƒٹپ[ƒjƒ“ƒO‚·‚é•K—v‚ھ‚ ‚é‚و‚¤‚ةژv‚ي‚ê‚é‚©‚à‚µ‚ê‚ـ‚¹‚ٌپB‚µ‚©‚µپAƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚ة‚و‚è–ٍچـ‘I‘ً‚âپAŒuŒُƒŒƒ|پ[ƒ^پ[‚ً“±“ü‚·‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پBGeneCopoeiaپiGCPپjژذ‚جƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚حپA–ٍچـ‘I‘ً‚âŒuŒُƒŒƒ|پ[ƒ^پ[ˆâ“`ژq‚ً‚à‚ء‚ؤ‚¢‚ـ‚·پiگ}.4پjپBƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“ŒمپAƒsƒ…پ[ƒچƒ}ƒCƒVƒ““™‚ج–ٍچـ‘¶چف‰؛‚ة‚¨‚¢‚ؤچ×–E‚ً’ل–§“x‚إ”dژي‚µپA’PˆêƒRƒچƒjپ[Œ`گ¬‚ً‘£‚µ‚ـ‚·پB‚ ‚é‚¢‚حپA96ƒEƒFƒ‹ƒvƒŒپ[ƒg‚ً—p‚¢‚ؤ’iٹKٹَژك‚ً‚ئ‚é•û–@‚à‚ ‚è‚ـ‚·پB–ٍچـ‘¶چف‰؛‚إگ¶’·‚·‚éƒRƒچƒjپ[‚ھپAڈCگ³•”•ھ‚ً•غژ‚·‚éˆہ’èچ×–Eٹ”چ\’zŒَ•â‚إ‚·پB
–ٍچـ‘دگ«‚âŒuŒُƒŒƒ|پ[ƒ^پ[”Œ»ƒNƒچپ[ƒ“‚ھ“¯’è‚إ‚«‚é‚ئپA‚»‚جŒم‚جژèڈ‡‚حNHEJپi”ٌ‘ٹ“¯––’[Œ‹چ‡پj‚ً—ک—p‚·‚éڈêچ‡‚ئŒ€“I‚ةˆظ‚ب‚è‚ـ‚·پBƒmƒbƒNƒAƒEƒg‚جڈêچ‡پA’تڈيپAƒZƒŒƒNƒVƒ‡ƒ“/ƒŒƒ|پ[ƒ^پ[ƒJƒZƒbƒg‚ھƒ^ƒ“ƒpƒNژ؟ƒRپ[ƒh—جˆو‚ة‘gچ‚ـ‚êپACRISPR-Cas9‚ة‚و‚èگط’f‚³‚ꂽ•”•ھ‚ة’Zچ½Œ‡‘¹‚ً‚à‚آ‚±‚ئ‚àژپX‚ ‚è‚ـ‚·پB‚»‚ج‘¼پADNA‚ج“ء’èگُگF‘ج—جˆو‚ھچيڈœ‚³‚êƒJƒZƒbƒg‚ئ’uٹ·‚³‚ê‚éڈêچ‡‚âˆâ“`ژq‚ھƒCƒ“ƒtƒŒپ[ƒ€‚ج—Zچ‡ƒ^ƒO‚ً•غ—L‚·‚éڈêچ‡‚à‚ ‚è‚ـ‚·پBƒXƒNƒٹپ[ƒjƒ“ƒO‚ًچs‚¤ڈêچ‡پA–¢ڈCگ³‚جگُگF‘ج”z—ٌ‚ئ‘}“ü”z—ٌ‚ئ‚ج‹«ٹE•”•ھ‚ة‚ـ‚½‚ھ‚éƒvƒ‰ƒCƒ}پ[‚ً—ک—p‚µ‚ؤPCR‚ًچs‚¢‚ـ‚·پB‘}“ü”z—ٌ‚جچ¶‚ئ‰E‘¤‚ج—¼•û‚ة‚¨‚¢‚ؤپAƒ}پ[ƒJپ[‚ئ“¯•ûŒü‚ةچ‡گ¬‚·‚é‚و‚¤‘ٹ“¯کr—p‚ة‚P‚آ‚جƒvƒ‰ƒCƒ}پ[‚ًگفŒv‚µپA”½‘خ‘¤‚جƒvƒ‰ƒCƒ}پ[‚ح‘ٹ“¯کr‚ةŒü‚©‚ء‚ؤچ‡گ¬‚·‚é‚و‚¤‘}“ü”z—ٌ‚ةگفŒv‚µ‚ـ‚·پB‚à‚µ‘gچ‚ف‚ھ—اچD‚ةچs‚ي‚ꂽڈêچ‡‚ة‚حپAƒAƒKƒچپ[ƒXƒQƒ‹ڈم‚إٹْ‘ز‚³‚ê‚é‘ه‚«‚³‚جƒoƒ“ƒh‚ًٹm”F‚·‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB
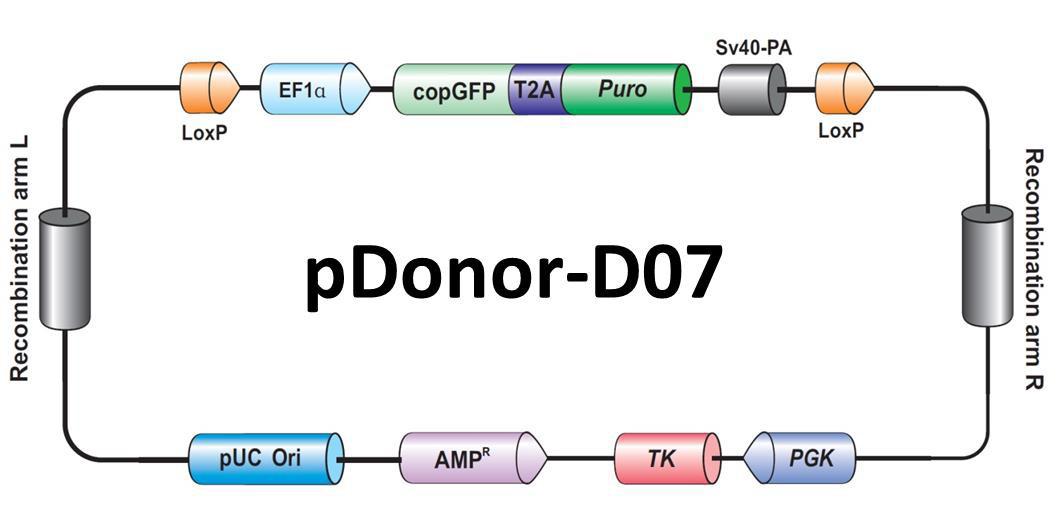
گ}.4پ@HRپiHDRپjƒAƒvƒٹƒPپ[ƒVƒ‡ƒ“—pGeneCopoeiaپiGCPپjژذƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚جˆê—ل
–ٍچـ‘I‘ً‚ًچs‚¤‚ئƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚جƒ‰ƒ“ƒ_ƒ€‘gچ‚ف‚ًڈµ‚‹°‚ê‚ھ‚ ‚èپAڈœٹO‚·‚é•K—v‚ھ‚ ‚è‚ـ‚·پBGeneCopoeiaپiGCPپjژذ‚جƒhƒiپ[ƒxƒNƒ^پ[‚ح‘gٹ·‚¦—جˆو‚جٹO‘¤‚ة’Pڈƒƒwƒ‹ƒyƒXƒEƒCƒ‹ƒXپiHSVپjƒ`ƒ~ƒWƒ“ƒLƒiپ[ƒ[پiTKپjˆâ“`ژq‚ً‚à‚ء‚ؤ‚¢‚ـ‚·پiگ}.4پjپBƒKƒ“ƒVƒNƒچƒrƒ‹‚ً“Y‰ء‚µ‚½‘I‘ً”|’n‚ًژg—p‚·‚é‚ئپAƒhƒiپ[ƒvƒ‰ƒXƒ~ƒh‚ھƒ‰ƒ“ƒ_ƒ€‚ة‘gچ‚ـ‚ꂽچ×–E‚ح’تڈيژ€–إ‚·‚邽‚كپAگ³ڈي‚بƒhƒiپ[‘gچ‚ف‚ھگ¶‚¶‚½چ×–EŒQ‚ً”Zڈk‚·‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB‚»‚ê‚ظ‚ا•p”ة‚إ‚ح‚ ‚è‚ـ‚¹‚ٌ‚ھپAƒ‰ƒ“ƒ_ƒ€‘gچ‚ف‚ة‚و‚èTKˆâ“`ژq‚ھ”rڈœ‚³‚ê‚邱‚ئ‚à‚ ‚邽‚كپAPCR‚âƒTƒUƒ“ƒuƒچƒbƒg‚ًچs‚ء‚ؤ‚±‚ê‚ç‚ًڈœ‹ژ‚·‚é‚ظ‚¤‚ھ‚و‚¢‚إ‚µ‚ه‚¤پB
چإŒم‚ةپAHRپiHDRپj‚ة‚و‚èڈCگ³‚³‚ꂽˆâ“`ژq‚حپAڈCگ³•”ˆتژü•س‚جگُگF‘جچ\‘¢‚ًٹm”F‚µپA“±“ü‚µ‚½•دˆظ‚ھ‘¶چف‚·‚邱‚ئ‚ًŒںڈo‚·‚邽‚كپAٹY“–‚·‚éڈêچ‡‚ة‚ح”z—ٌŒˆ’è‚·‚é•K—v‚ھ‚ ‚è‚ـ‚·پB ڑM“û“®•¨چ×–EƒVƒXƒeƒ€‚ة‚¨‚¯‚éCRISPR-Cas9‚جƒfƒUƒCƒ“پAچ\’z‚¨‚و‚ر‚»‚ج—ک—p‚ةٹض‚·‚éگê–ه’mژ¯‚âŒoŒ±‚ة•x‚قGeneCopoeiaپiGCPپjژذ‚إ‚حپAsgRNA‚âHDRƒhƒiپ[ƒfƒUƒCƒ“‚©‚çچى‹ئ‚ًٹJژn‚µپA”z—ٌŒںڈطچد‚فƒvƒ‰ƒXƒ~ƒh‚ً‚²’ٌ‹ں‚µ‚ؤ‚¢‚ـ‚·پB‚ـ‚½پACRISPR-Cas9چ\’z‚â‹@”\Œںڈط‚ب‚ا‚جƒJƒXƒ^ƒ€ƒTپ[ƒrƒX‚à‚²’ٌ‹ں‚µ‚ؤ‚¢‚ـ‚·پB
ƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚âƒXƒNƒٹپ[ƒjƒ“ƒOŒv‰و‚ًچl‚¦‚é‘O‚ةپAƒXƒNƒٹپ[ƒjƒ“ƒO‚·‚éƒRƒچƒjپ[گ”‚ة‰e‹؟‚ً‹y‚ع‚·‰آ”\گ«‚ھ‚ ‚é•،گ”‚ج—vˆِ‚âپA•K—v‚بڈêچ‡‚ة‚حŒJ•ش‚µژہژ{‚·‚éƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚ج‰ٌگ”‚ةٹض‚µ‚ؤڈnچl‚·‚é•K—v‚ھ‚ ‚è‚ـ‚·پB
پ، ƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦
CRISPR-Cas9 ƒQƒmƒ€•زڈWƒcپ[ƒ‹‚ًژَ‚¯ژو‚é‚إ‚ ‚낤چ×–E‚جٹ„چ‡‚حپAƒXƒNƒٹپ[ƒjƒ“ƒO‚ًچs‚¤ƒRƒچƒjپ[گ”‚ًŒˆ’è‚·‚éڈم‚إ”ٌڈي‚ةڈd—v‚إ‚·پB‚à‚µژg—pچ×–Eٹ”‚ة‚¨‚¯‚éƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦‚ھ40%‚جڈêچ‡پAƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦‚ھ80پ“‚جچ×–E‚ة”ن‚ׂؤ2”{‚à‚جگ”‚جƒRƒچƒjپ[‚ًƒXƒNƒٹپ[ƒjƒ“ƒO‚·‚邱‚ئ‚ھ—\‘z‚³‚ê‚ـ‚·پB‚à‚µژg—pچ×–Eٹ”‚جƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦‚ھ’ل‚¢ڈêچ‡پAƒvƒ‰ƒXƒ~ƒh‚ةƒRپ[ƒh‚³‚ꂽŒuŒُƒ}پ[ƒJپ[‚ًژg‚ء‚ؤƒ\پ[ƒeƒBƒ“ƒO‚µ‚ؤƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚³‚ꂽچ×–E‚ً”Zڈk‚µ‚½‚èپA’Zٹْ“I‚ة‚ح–ٍچـ‘I‘ً‚ً—ک—p‚·‚邱‚ئ‚à‚إ‚«‚ـ‚·پBGFP‚ًژn‚ك‚ئ‚·‚éŒuŒُƒŒƒ|پ[ƒ^پ[‚ً’èڈي”Œ»‚·‚éƒvƒ‰ƒXƒ~ƒh‚ً—ک—p‚µ‚ؤژg—pچ×–Eٹ”‚جƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦‚ًگ„’è‚·‚邱‚ئ‚ًگ„ڈ§‚µ‚ـ‚·پB
پ، ƒRƒsپ[گ”
ٹ®‘S‚بƒmƒbƒNƒAƒEƒg‚â•دˆظ—U”گ«‚ً“¾‚邽‚ك‚ة‚حپA•W“Iˆâ“`ژq‚ج‘S‚ؤ‚ج‘خ—§ˆâ“`ژq‚ًڈCگ³‚·‚é•K—v‚ھ‚ ‚é‚©‚à‚µ‚ê‚ـ‚¹‚ٌپB“ٌ”{‘جچ×–Eٹ”‚ًژg—p‚·‚éڈêچ‡پA2‚آ‚ج‘خ—§ˆâ“`ژq‚ًڈCگ³‚·‚é•K—vگ«‚ھ‚ ‚é‚ئ‘z’è‚·‚錤‹†ژز‚ھ‘½‚‚¢‚ـ‚·پB‚µ‚©‚µپAHeLa‚ًژn‚ك‚ئ‚·‚éˆê”ت“I‚ب•sژ€‰»چ×–Eٹ”‚ج‘½‚‚حپAˆظگ”‘ج‚ـ‚½‚ح”{گ”‘ج‚إ‚ ‚邽‚كپA‘خڈغˆâ“`ژq‚ً2ƒRƒsپ[ˆبڈم•غ—L‚µ‚ؤ‚¢‚é‰آ”\گ«‚ھ‚ ‚è‚ـ‚·پB1‚آ‚جچ×–E“à‚إ‚حپA•،گ”‚ج‘خ—§ˆâ“`ژqڈCگ³‚ة”ن‚ׂؤ’Pˆê‘خ—§ˆâ“`ژqڈCگ³Œّ—¦‚ج•û‚ھچ‚‚‚ب‚è‚ـ‚·پB‚µ‚½‚ھ‚ء‚ؤپA‚à‚µ2‚آˆبڈم‚ج‘خ—§ˆâ“`ژq‚ًڈCگ³‚·‚é•K—v‚ھ‚ ‚éڈêچ‡‚ة‚حپA2‘خ—§ˆâ“`ژqڈCگ³‚ة”ن‚ׂؤ‚و‚葽‚‚جƒRƒچƒjپ[‚ًƒXƒNƒٹپ[ƒjƒ“ƒO‚·‚é•K—v‚ھ‚ ‚é‚ئچl‚¦‚ç‚ê‚ـ‚·‚ج‚إپA•،گ”‰ٌ‚ة‚ي‚½‚ء‚ؤƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚ًچs‚¤•K—v‚ھ‚ ‚é‚©‚à‚µ‚ê‚ـ‚¹‚ٌپB
پ، گط’fŒّ—¦
CRISPR-Cas9‚ة‚و‚é‘}“üŒ‡‘¹Œ`گ¬Œّ—¦‚حپA’تڈيپA–ٌ5پ“پ`70پ“‚إ‚·پBƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦‚جڈêچ‡‚ئ“¯—l‚ةپAگط’fŒّ—¦‚ھ40پ“‚جڈêچ‡‚ة”ن‚×پA‚»‚ê‚ھ20پ“‚جڈêچ‡‚ح2”{‚ظ‚ا‚جگ”‚جƒRƒچƒjپ[ƒXƒNƒٹپ[ƒjƒ“ƒO‚ھ—\‘ھ‚³‚ê‚ـ‚·پB
ڈCگ³ƒNƒچپ[ƒ“‚ً“¯’è‚·‚邽‚ك‚جƒXƒNƒٹپ[ƒjƒ“ƒO‚ةژg—p‚·‚é‚ׂ«ƒRƒچƒjپ[گ”‚حپAژg—p‚·‚éچ×–E—R—ˆ‚ج—vˆِ‚âپA—vˆِ‚ج‘gچ‡‚¹‚ةˆث‘¶‚µ‚ـ‚·پB’PڈƒŒvژZ‚·‚é‚ئپA‚à‚µ50%‚جگط’fŒّ—¦‚ً‚à‚آCRISPR-Cas9 ƒQƒmƒ€•زڈWƒcپ[ƒ‹‚ً—p‚¢‚ؤƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“Œّ—¦‚ھ60%‚ج“ٌ”{‘جچ×–Eٹ”‚ج2‘خ—§ˆâ“`ژqƒmƒbƒNƒAƒEƒg‚ً“¾‚½‚¢ڈêچ‡پA’Pˆê‘خ—§ˆâ“`ژq‚ھڈCگ³‚³‚ꂽƒRƒچƒjپ[‚جٹ„چ‡‚ح0.5 × 0.6 = 30%‚ئ‚ب‚è‚ـ‚·پB2‘خ—§ˆâ“`ژqڈCگ³‚جڈêچ‡پA—zگ«ƒRƒچƒjپ[‚جٹ„چ‡‚ح15%‚ئ‚ب‚è‚ـ‚·پBˆبڈم‚ًچl—¶‚·‚é‚ئپA2‘خ—§ˆâ“`ژqڈCگ³‚ً‚à‚آƒNƒچپ[ƒ“‚ً‚P‚آ“¯’è‚·‚邽‚ك‚ة‚حڈ‚ب‚‚ئ‚à20‚جƒRƒچƒjپ[ƒXƒNƒٹپ[ƒjƒ“ƒO‚ھ•K—v‚ئ‚ب‚è‚ـ‚·پB‚à‚µپAƒgƒ‰ƒ“ƒXƒtƒFƒNƒVƒ‡ƒ“‚ئگط’fŒّ—¦‚ھ‚و‚è’ل‚¢ڈêچ‡‚إپAژg—pچ×–Eٹ”‚ة•W“Iˆâ“`ژq‚ھ2ƒRƒsپ[ˆبڈم‘¶چف‚·‚éڈêچ‡پA‚ي‚¸‚©‚P‚آ‚جٹ®‘S‚بƒmƒbƒNƒAƒEƒgچ×–E‚ً’P—£‚·‚邽‚ك‚ةپA‚و‚葽‚‚جƒRƒچƒjپ[ƒXƒNƒٹپ[ƒjƒ“ƒO‚ھ•K—v‚ئ‚ب‚è‚ـ‚·پB