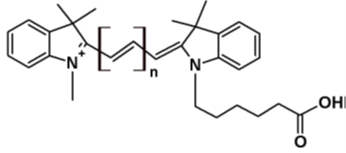
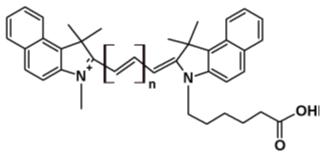
シアニン色素は、蛍光色素として特にバイオメディカルイメージングに多く利用されています。
構造によって、可視領域や近赤外領域のスペクトルをカバーします。Cy3®、Cy5®、Cy7®は、最も一般的なシアニン系色素です。Cy3®はオレンジ色の蛍光(〜550/570 nm)を持ち、Cy5®は赤色領域(〜650/670 nm)で蛍光を発します。Cy3®とCy5®は、通常 2色検出のために組み合わされ使用されています。
これらは通常、核酸またはタンパク質分子に化学的に結合できるように、窒素側鎖の一方または両方に反応基を持つように合成されます。
標識は可視化や定量目的で行われます。Cy3® や Cy5®は、ゲノムハイブリダイゼーションやトランスクリプトミクスに使用される遺伝子チップなど、幅広い用途で使用されています。また、プロテオミクスやRNA局在を含む様々な研究のためのタンパク質や核酸の標識にも使用されています。
スルホン化 vs 非スルホン化シアニン
スルホン化シアニン色素と非スルホン化シアニン色素は非常によく似た蛍光特性を示すので、多くの用途で互換性を持って使用することができます。
両者の違いは、主にその溶解性にあります。非スルホン化シアニン色素 (図2) は、生体分子を標識する前に、DMFやDMSOなどの有機共溶媒に溶解させる必要があります。一方、スルホン化シアニン (図1) は水系溶媒で使用できます(帯電したスルホン酸基が色素やコンジュゲートの凝集を抑制します)。
水または水系バッファーを用いた透析による精製では、未反応色素を効率的に除去するためにスルホン化シアニンを使用する必要がございます。ゲルろ過、クロマトグラフィー、電気泳動による精製は、スルホン化シアニン、非スルホン化シアニンのいずれでも可能です。
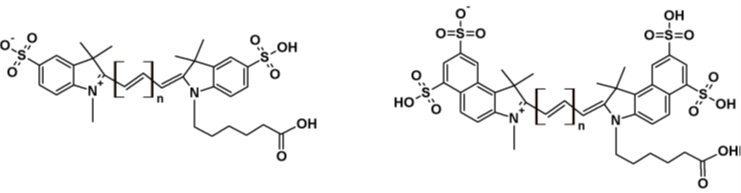
図1 オリゴヌクレオチドを標識するためのスルホン化シアニン色素の化学構造。
(左:Cy3®:n=1、Cy5®:n=2、Cy7®:n=3。右図 Cy3.5®: n=1; Cy5.5®: n=2; Cy7.5®: n=3)。
| Cy3® | Cy5® | Cy7® | ||||
|---|---|---|---|---|---|---|
| Form | Sulfo | Non-Sulfo | Sulfo | Non-Sulfo | Sulfo | Non-sulfo |
| Ex/Em (nm) | 554/568 | 650/669 | 754/778 | |||
| Filter Set | Cy/TRITC | Cy5 | Cy7 | |||
| ε | 150,000 | 140,000 | 250,000 | 230,000 | 250,000 | 250,000 |
| φ | 0.1 | 0.07 | 0.27 | 0.16 | 0.12 | 0.2 |
| 品番 | 263 | 191 | 268 | 195 | 161 | 198 |
ε: is the extinction coefficient (cm-1M-1).
φ: is the fluorescence quantum yield.
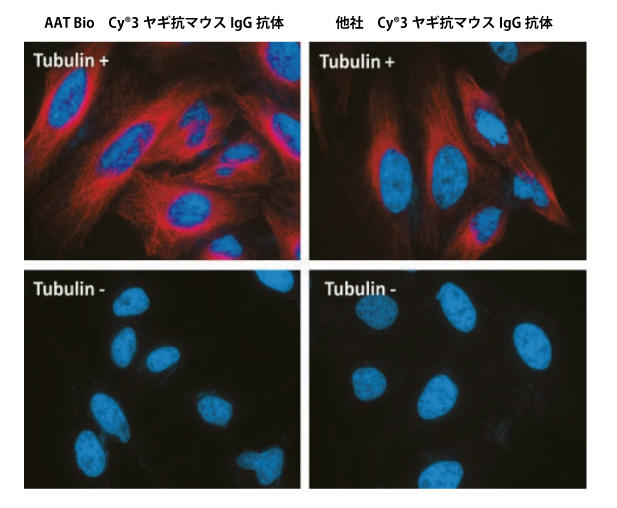
HeLa細胞をTublin(+)またはTublin(-)マウス抗チューブリンIgG抗体でインキュベート後、AATバイオクエスト社及び他社のCy®3標識ヤギ抗マウスIgG抗体を用いて検出した。核はHoechest33342で染色した。
| Succinimidyl Ester/NHS esters | 抗体、タンパク質、ペプチド、アミン修飾オリゴヌクレオチドのアミン (-NH2) への標識 |
|---|---|
| maleimide | 抗体、タンパク質、ペプチドのスルフヒドリル基 (-SH) への標識 |
| Azides | クリックケミストリーを使ったエチレン基への標識 |
| Alkynes | クリックケミストリーを使った azide への標識 |
| Hydrazides | アルデヒド基やケトン基への標識 |
| Carboxylic acids | カルボジイミドによる活性化後のアミンまたはアルコールのシュテークリヒエステル化への標識用に |
| Amines | 活性エステルなどのさまざまな求電子性化合物への標識 |























 このページを印刷する
このページを印刷する