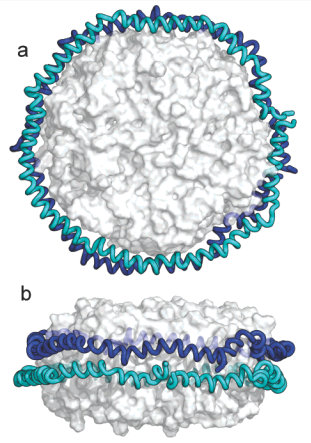
ナノディスク技術は、構造研究をはじめ、構造生物学、電子顕微鏡、NMR、EPR、および分光測定検出といった様々な技術分野に適用することができます。
| 特色とアプリケーション |
実験手法 |
膜タンパク質 |
| 可溶化と安定化 |
X線結晶解析
NMR
共鳴ラマンスペクトル法
光学吸収
EPR
無細胞発現 |
GPCR
さまざまな膜タンパク質
チトクロムP450
チトクロムP450とロドプシン
トランスポータとロドプシン
多様 |
| 足場タンパク質や脂質上の親和性タグを用いた表面固定化 |
単分子研究、SPR、LSPRおよび感知と検出 |
チトクロムP450、GPCR、および血液凝固第VII因子 |
| 単量体単離、多量体、および複数タンパク質の機能的複合体 |
構造および機能研究 |
受容体とロドプシン
CPRとATPaseを含むチトクロムP450 |
| 構造的に均質な調製 |
SAXSとSANS
EM |
チトクロムP450と還元酵素
受容体とチャネル |
| 大きさ、電荷、または密度による分画 |
クロマトグラフィ、電気泳動、および超遠心 |
多様 |
| タンパク質-膜間結合 |
SPR |
K-Rasタンパク質、TF-VIIaおよびPgPトランスポータ |
| タンパク質の性質への膜効果 |
酸化還元電位
動態学 |
チトクロムP450還元酵素
血液凝固第VIII因子
呼吸器複合体 |
表.1 ナノディスクに抱合された膜タンパク質に使用された手法やツール
SPR: 表面プラズモン共鳴; LSPR: 局在化SPR; CPR: NADPH-チトクロムP450還元酵素[5].
In Vitro E.coliタンパク質発現とナノディスク技術を用いたアクアポリン発現
WUHAN HUAMEI BIOTECH社では、in vitro E.coli タンパク質発現とナノディスク技術を組み合わせ、あらかじめ合させたナノディスクをin vitro E.coli タンパク質発現システムに取り入れました。膜タンパク質の翻訳ステップでにこれをナノディスクに会合させ、膜タンパク質 - ナノディスク複合体を形成させました(図2)。この疑似的人工脂質環境は、膜タンパク質に対するさまざまな脂質の影響を分析する新規の手段となり、膜タンパク質の研究に役立ちます。
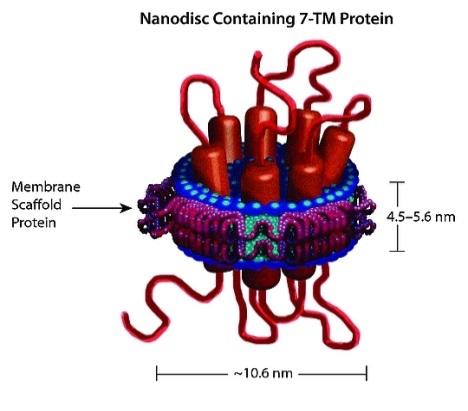
図.2 7つの膜貫通タンパク質が包埋されたMSPナノディスクの模式図
直径:およそ10.6 nm。
* Picture from Sligar.
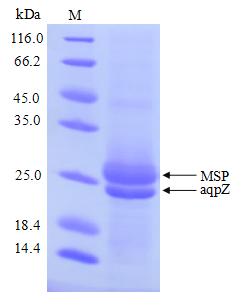
図.3 ナノディスクとE.coli アクアポリンZ(aqpZ)を良好に会合した後のSDS-PAGE結果
図2に示したように、MSPと標的タンパク質である膜タンパク質aqpZの2つのバンドが確認できる。
参考文献
- Applications of Phospholipid Bilayer Nanodiscs in the Study of Membranes and Membrane Proteins. Abhinav Nath, William M. Atkins, and Stephen G. Sligar. Biochemistry, 2007, 46 (8), 2059-2069
- Large volume liposomes by an ether vaporization method. D Deamer, AD Bangham. Biochimica et Biophysica Acta, 443 (1976) 629-~34
- Applications of Phospholipid Bilayer Nanodiscs in the Study of Membranes and Membrane Proteins. Abhinav Nath, William M. Atkins, and Stephen G. Sligar. Biochemistry, 2007, 46 (8), 2059-2069
- Self-assembly of discoidal phospholipid bilayer nanoparticles with membrane scaffold proteins. Timothy H. Bayburt,Yelena V. Grinkova, and Stephen G. Sligar. Nano Letters, 2002, 2 (8), pp 853-856
- Nanodiscs for structural and functional studies of membrane proteins.Ilia G Denisov & Stephen G Sligar. Nature Structural & Molecular Biology 23, 481-486 (2016)























 このページを印刷する
このページを印刷する