Solulink(ソルリンク)社のタンパク質−タンパク質結合キットは、簡単・効率的に2つのタンパク質を結合することができます。
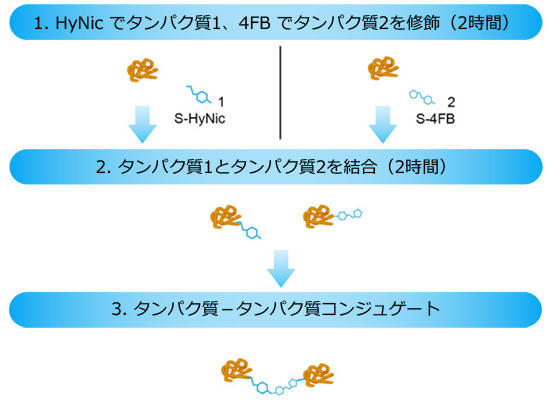
経験が少ない方、または、初めて行う方でも、必要に応じたタンパク質−タンパク質コンジュゲートを柔軟に作製することが可能です。キットには、必要なコンポーネント(S-HyNic および S-4FB を含む)全てと、7 kDa 以上のサイズのタンパク質を簡単・特異的に架橋するためのプロトコールが含まれています。
Solulink(ソルリンク)社のタンパク質−タンパク質結合キットは、簡単・効率的に2つのタンパク質を結合することができます。
経験が少ない方、または、初めて行う方でも、必要に応じたタンパク質−タンパク質コンジュゲートを柔軟に作製することが可能です。キットには、必要なコンポーネント(S-HyNic および S-4FB を含む)全てと、7 kDa 以上のサイズのタンパク質を簡単・特異的に架橋するためのプロトコールが含まれています。
ソルリンク社独自の、触媒作用によるヘテロ二官能性リンカー技術は、非常に簡単で高効率な手法です。作製したコンジュゲートは、UVによる追跡が可能で、安定した結合 (bis-arylhydrazone)を有し 、354 nm の吸光度で測定できます。
ソルリンク社のバイオコンジュゲーション法は、TurboLink™ 触媒を、タンパク質の2モル当量以上添加した場合、95% 以上のタンパク質がコンジュゲートに転換されます。変換率が高く、UVによる追跡が可能なことから、FPLC やダイアフィルトレーションなどのサイズ排除による精製法を用いて、過剰なタンパク質からコンジュゲートを簡単に精製・同定することができます。キットには反応2回分の試薬が含まれており、4時間以内の反応で、 40–60% のコンジュゲート(精製後)を得ることができます。作製したコンジュゲートは、ELISA、フローサイトメトリー、IHC、イムノアッセイなどに使用できます。
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Protein-Protein Conjugation Kit |
SLK | S-9010-1 | 1 KIT |
販売終了 |
【関連商品】
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について
© COSMO BIO