Genocel® シートタイプ
- 【1】 Genocel® の原材料、基礎特性について
- 【2】 膨潤、細胞シート剥離、培養について
- 【3】 観察・評価方法について
- 【4】 Genocel® のカスタマイズについて
- 【5】 応用について
Genocel® ブロックタイプ
Genocel® パウダータイプ
【1-01】 原材料は何ですか?
材料は牛骨由来ゼラチンと水のみです。架橋剤は使っていません。
【1-02】 動物成分は入っていますか?
牛骨由来のゼラチンを使用しております。ゼラチンはアルカリ、高温処理で抽出、精製されており、高度精製品に分類されるため、厚労省の生物由来原料基準の対象外となっています。
【1-03】 細胞毒性はありますか?
コロニー形成阻害試験で陰性であり、細胞毒性作用なしとなっております。
【1-04】 分解期間はどのくらいですか?
細胞なしの液体培地中で、55 日以上、形状維持することを確認しております。細胞培養により、細胞が増えてくると細胞が産生する分解酵素 (マトリクスメタロプロテアーゼ:MMP)で分解されていくと考えられます。
【2-01】 膨潤したサンプルを再使用できますか?
1 度膨潤させたサンプルは、使い切りとしてください。膨潤後の再使用は推奨いたしません。
【2-02】 開封後、再滅菌することはできますか?
再滅菌後の物性等について保証いたしかねますので、再滅菌はできません。
【2-03】 細胞シートの培養皿からの剥離をどのように行いますか?
ピペッティングによる液流で剥離させるか、温度感応性培養皿をご使用ください。
【2-04】 どのような培養方法を用いますか?
通常の静置培養に加えて、培養皿をシェイカー上に置いておこなう旋回培養の実施例があります。 静置培養よりも旋回培養の方が、Genocel® 内部への細胞侵入、増殖が早くなります。
【2-05】 どのような細胞で培養可能ですか?
ヒト間葉系幹細胞(hMSC)、マウス繊維芽細胞(MC3T3-E1、3T3-L1、L929)、マウス間葉系幹細胞様細胞(KUM6)、ラット骨髄より採取した MSC、ヒト乳腺上皮細胞(EpH4V)、ヒト胎児腎細胞(HEK293)での培養を確認しております。 EpH4V ではGenocel ®との接着性は他の細胞と比較して低い傾向があります。
【3-01】 培養中の細胞の観察方法は?
明視野、蛍光とも、ディッシュやウェルプレート内で培養中の足場表面を観察可能です。培養液中あるいは、PBS 中で観察してください。尚、明視野観察では、細胞が足場内部まで密に増殖すると、透明性がなくなるため、観察しにくくなります。位相差顕微鏡でも観察可能です。
【3-02】 培養後に切片作製が可能ですか。組織染色に推奨なプロトコルはありますか?
切片作製が可能です。凍結包埋し、5 - 15 µm 厚で切片を作製してください。封入なしもしくは非水溶性封入剤でも観察可能ですが、水溶性封入剤で封入する方が、より膨潤状態に近い状態での観察像が得られます。
【3-03】 Genocel® から細胞を分離できますか?
トリプシンEDTA溶液または、コラゲナーゼ/PBS+溶液に投入し、37℃でインキュベートすることで、ゼラチン成分を溶かすことができます。トリプシンEDTA溶液は、細胞をはがすために一般的に使われている濃度のものをご使用いただけます。トリプシン EDTA 溶液をご使用される場合は、分離後に培地を添加し、反応を止めてください。コラゲナーゼについては、適切な濃度をご検討ください。処理前に Genocel® を細断するか、積極的に攪拌を行うことで、細胞とゼラチンの分離を促進することが可能です。また必要により、上清を除去した後に、PBS で再懸濁することで、洗浄を行ってください。
【4-01】 分解期間をコントロールできますか?
お問い合わせください。
【4-02】 密度や孔径の異なる Genocel® を製造できますか?
お問い合わせください。
【4-03】 現行サイズ以外の大きさの Genocel® を製造できますか?
受注対応となります。お問い合わせください。
【6-01】 原材料は何ですか?
材料は牛骨由来ゼラチンと水のみです。架橋剤は使っていません。
【6-02】 動物成分は入っていますか?
牛骨由来のゼラチンを使用しております。ゼラチンはアルカリ、高温処理で抽出、精製されており、高度精製品に分類されるため、厚労省の生物由来原料基準の対象外となっています。
【6-03】 細胞毒性はありますか?
コロニー形成阻害試験で陰性であり、細胞毒性作用なしとなっております。
【6-04】 分解期間はどのくらいですか?
細胞なしの液体培地中で、55 日以上、形状維持することを確認しております。細胞培養により、細胞が増えてくると細胞が産生する分解酵素 (マトリクスメタロプロテアーゼ:MMP)で分解されていくと考えられます。
【7-01】 膨潤したサンプルを再使用できますか?
1 度膨潤させたサンプルは、使い切りとしてください。膨潤後の再使用は推奨いたしません。
【7-02】 開封後、再滅菌することはできますか?
再滅菌後の物性等について保証いたしかねますので、再滅菌はできません。
【7-03】 細胞の接着、増殖挙動は?
・細胞の多くが、Genocel® の繊維交点に付着します。培養日時の経過により、繊維に沿った細胞の変形や、繊維に沿った増殖がみられます。
【7-04】 細胞播種方法の違いは?
静置播種よりも、振盪播種を用いた方が、足場内部に細胞が侵入しやすくなります。増殖細胞では、培養日時の経過により、播種方法による差は少なくなります。
【7-05】 培養方法の違いは?
静置培養よりも、旋回培養もしくは撹拌培養の方が、Genocel® 内部への細胞侵入、増殖が早くなります。
【7-06】 どのような細胞で培養可能ですか?
ヒト間葉系幹細胞(hMSC)、マウス繊維芽細胞(MC3T3-E1、3T3-L1、L929)、マウス間葉系幹細胞様細胞(KUM6)、ラット骨髄より採取した MSC、ヒト乳腺上皮細胞(EpH4V)、ヒト胎児腎細胞(HEK293)での培養を確認しております。 EpH4V ではGenocel ®との接着性は他の細胞と比較して低い傾向があります。
【8-01】 培養中の細胞の観察方法は?
明視野、蛍光とも、ディッシュやウェルプレート内で培養中の足場表面を観察可能です。培養液中あるいは、PBS 中で観察してください。尚、明視野観察では、細胞が足場内部まで密に増殖すると、透明性がなくなるため、観察しにくくなります。位相差顕微鏡でも観察可能です。
【8-02】 培養後に切片作製が可能ですか。組織染色に推奨なプロトコルはありますか?
切片作製が可能です。凍結包埋し、5 - 15 µm 厚で切片を作製してください。封入なしもしくは非水溶性封入剤でも観察可能ですが、水溶性封入剤で封入する方が、より膨潤状態に近い状態での観察像が得られます。
【8-03】 Genocel® から細胞を分離できますか?
トリプシンEDTA溶液または、コラゲナーゼ/PBS+溶液に投入し、37℃でインキュベートすることで、ゼラチン成分を溶かすことができます。トリプシンEDTA溶液は、細胞をはがすために一般的に使われている濃度のものをご使用いただけます。トリプシン EDTA 溶液をご使用される場合は、分離後に培地を添加し、反応を止めてください。コラゲナーゼについては、適切な濃度をご検討ください。処理前にGenocel® を細断するか、積極的に攪拌を行うことで、細胞とゼラチンの分離を促進することが可能です。また必要により、上清を除去した後に、PBS で再懸濁することで、洗浄を行ってください。
【9-01】 分解期間をコントロールできますか?
お問い合わせください。
【9-02】 密度や孔径の異なる Genocel® を製造できますか?
お問い合わせください。
【9-03】 現行サイズ以外の大きさの Genocel® を製造できますか?
受注対応となります。お問い合わせください。
【10-01】 臨床に使用できますか?
本品は、研究用として製造しております。臨床用途には使用できません。
【11-01】 原材料は何ですか?
材料は牛骨由来ゼラチンと水のみです。架橋剤は使っていません。
【11-02】 動物成分は入っていますか?
牛骨由来のゼラチンを使用しております。ゼラチンはアルカリ、高温処理で抽出、精製されており、高度精製品に分類されるため、厚労省の生物由来原料基準の対象外となっています。
【11-03】 細胞毒性はありますか?
コロニー形成阻害試験で陰性であり、細胞毒性作用なしとなっております。
【11-04】 分解期間はどのくらいですか?
細胞なしの液体培地中で、55 日以上、形状維持することを確認しております。細胞培養により、細胞が増えてくると細胞が産生する分解酵素 (マトリクスメタロプロテアーゼ:MMP)で分解されていくと考えられます。
【11-05】 パウダーのサイズはどの程度ですか?
膨潤時の繊維径は約 50 µm、繊維長は 200〜300 µm を平均として分布があります。
【12-01】 膨潤したサンプルを乾燥して再使用できますか?
1 度膨潤させたサンプルは、使い切りとしてください。膨潤後の再使用は推奨いたしません。
【12-02】 開封後、再滅菌することはできますか?
再滅菌後の物性等について保証いたしかねますので、再滅菌はできません。
【12-03】 どのような細胞で培養可能ですか?
ヒト間葉系幹細胞(hMSC)、マウス線維芽細胞(MC3T3-E1)、マウス間葉系幹細胞様細胞(KUM6)での培養を確認しております。
【13-01】乾燥したパウダーを分取するとき、静電気でチューブやスパーテルにくっつきます。
帯電防止チューブ(イナ・オプティカ製 AS-0150R など)、帯電防止型スパーテル(イナ・オプティカ製 AS-1800S など)を使用するとチューブやスパーテルへのパウダーの付着が抑えられます。製品用のチューブは帯電防止チューブを使用しています。

【13-02】パウダーを懸濁する際に、ピペットチップやチューブにパウダーが付着します。
水、PBS、無血清培地で懸濁するとピペットチップやマイクロチューブに付着します。血清入り培地(目安として血清1%以上) で懸濁させることで付着が抑えられます。血清入り培地を使用できない場合は、血清入り培地や牛血清アルブミン水溶液 (目安として 0.5%以上)でピペットチップやチューブを数回リンスしてください。付着が抑えられます。
【14-01】 どのような方法でスフェロイドを作製しますか?
細胞非接着性の U 底の 96 ウェルプレートを用いて作製します。例として Corning®スフェロイドマイクロプレート 96 well、住 友ベークライト PrimeSurface®96U でのスフェロイド形成を確認しています。一方で、一般的な浮遊培養用 96 ウェルプレートではスフェロイドは形成しませんでした。そのようなウェルプレートの場合、PVA のコーティングが必要です。また、マイクロパターニ ングの培養皿は、マイクロパターンにパウダーが入らないため、使用できません。
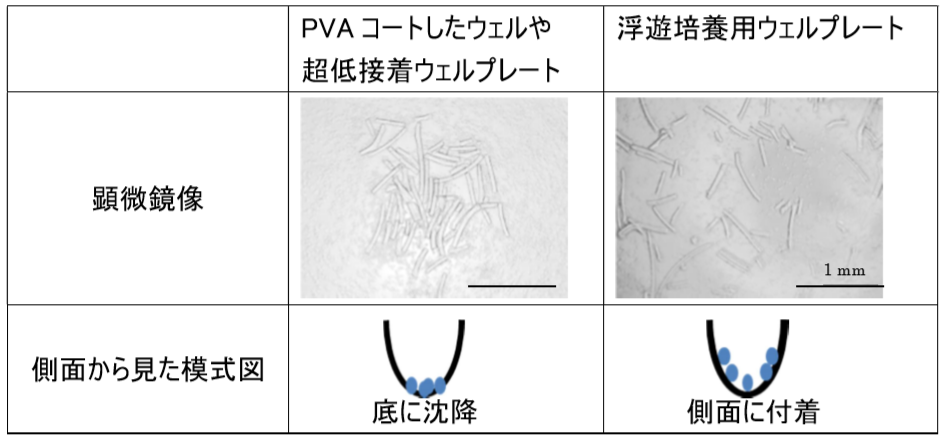
【14-02】 ウェルプレートに加えたパウダーがウェルの U 底に沈降しません。パウダーがウェルの側面に付着します。
【14-03】 96 ウェルプレートからスフェロイドを回収できますか。
マイクロピペットを用いて回収できます。その際、スフェロイドのサイズより大きな開口径のピペットチップをご使用ください。 3T3-E1 細胞の例では、ピペッティングを行ってもスフェロイドが崩壊しないことを確認しています。
【14-04】 スフェロイドのサイズはどのようにコントロールできますか。
細胞播種密度と、パウダーの添加量を変えることで形成されるスフェロイドのサイズをコントロール可能です。傾向としては、パ ウダーの添加量を多くするとスフェロイドのサイズが大きくなる、もしくは疎なスフェロイドが形成します。加えてパウダーの添加量 を多くするとスフェロイドの形成時間が長くなります。
【14-05】 どのように培地交換をしますか。
培地の半量交換をお勧めします。例えば、96 ウェルプレートで 1 ウェルあたり 200 ?L の培地で培養した場合、100 ?L の培地を吸引し、100 ?L の新しい培地を添加します。そのときスフェロイドの吸引や崩壊を防ぐために、培地交換はウェルの中心を避け、ウェルの端を使って培地の吸引と添加をすることをお勧めします。
【15-01】 培養後に切片作製が可能ですか。組織染色に推奨なプロトコルはありますか?
切片作製が可能です。凍結包埋し、5 - 15 µm 厚で切片を作製してください。封入なし、もしくは非水溶性封入剤の場合は脱水によってパウダーが収縮した像が観察されます。水溶性封入剤で封入すると、パウダーの膨潤状態に近い状態で観察でき ます。
【15-02】 Genocel® から細胞を分離できますか?
トリプシン EDTA 溶液または、コラゲナーゼ/PBS(+)溶液に投入し、37℃でインキュベートすることで、ゼラチン成分を溶かすことができます。トリプシン EDTA 溶液は、細胞をはがすために一般的に使われている濃度のものをご使用いただけます。トリプシン EDTA 溶液をご使用される場合は、分離後に培地を添加し、反応を止めてください。コラゲナーゼについては、適切な濃度をご検討ください。処理中にピペッティングや、積極的に攪拌を行うことで、細胞とゼラチンの分離を促進することが可能です。また必要により、上清を除去した後に PBS で再懸濁することで洗浄を行ってください。
【16-01】 分解期間をコントロールできますか?
お問い合わせください。
【16-02】 繊維径や繊維長の異なる Genocel® を製造できますか?
お問い合わせください。
【17-01】 臨床に使用できますか?
本品は、研究用として製造しております。臨床用途には使用できません。