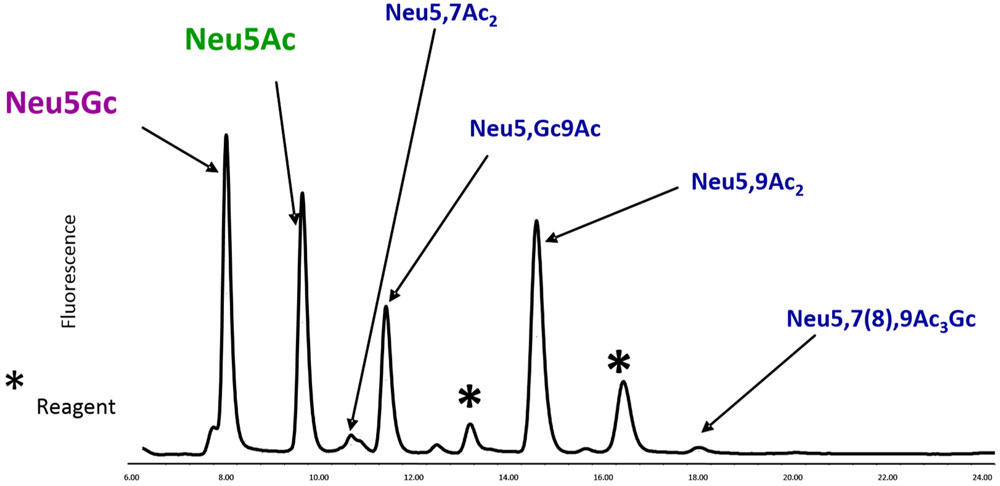
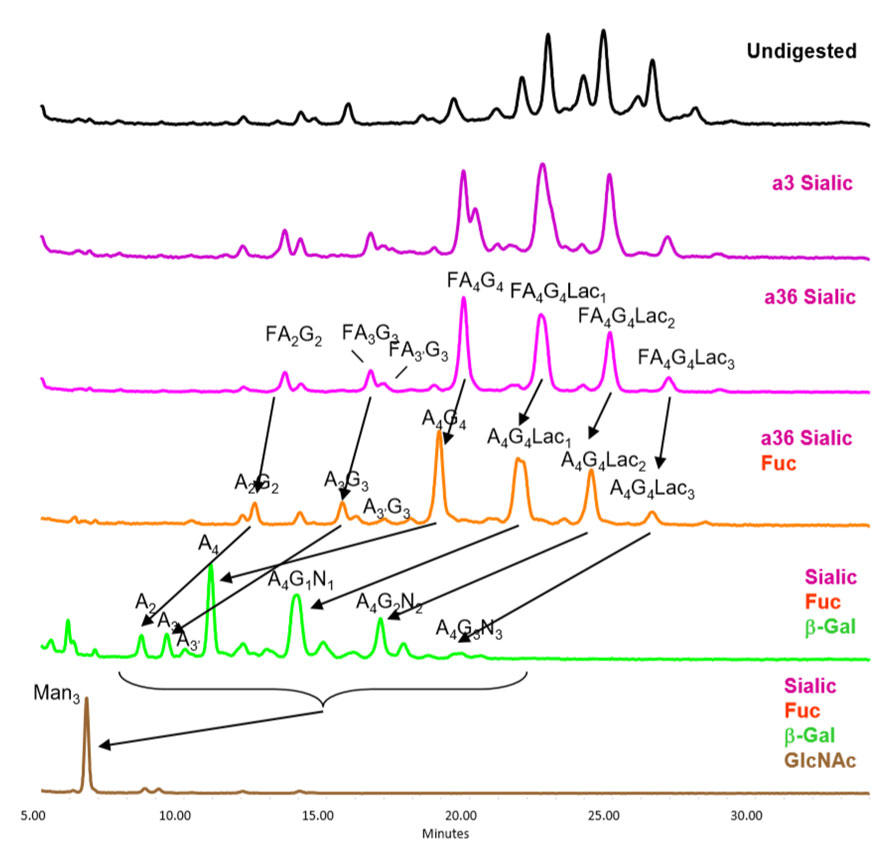
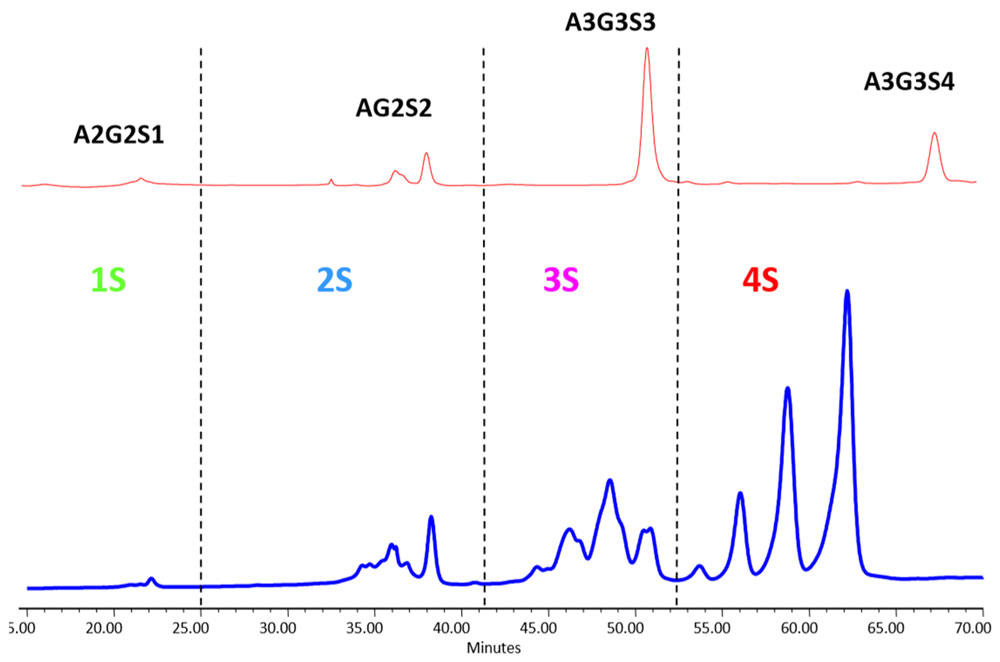
ヒトにおいて、グリカン上の主要なシアル酸はNeu5Acですが、非ヒト細胞株を用いて発現させた場合、Neu5Gcが糖タンパク質に付与されることがあります。この非ヒトNeu5Gcは炎症や、バイオ医薬品の中和(有効性の喪失)といった免疫学的応答を誘発する可能性があります。また、グリカンのシアル化は、薬物動態にも大きな影響を及ぼし得ます。シアル酸を失い、末端にガラクトースが露出した糖タンパク質は、肝臓内のアシアロ糖タンパク質受容体によって血中から除去されることが知られています。例えばEPOは、シアル酸に余分なアセチル化修飾(Neu5,9Ac2)を受けることで、薬効(半減期)に影響が出ます。また、糖鎖のシアル化は、受容体結合およびシグナル伝達にとっても重要であり、例えばIgG Fcのグリカンにシアル酸が存在すると、ADCC(抗体依存性細胞傷害)活性が低下することや、それをマウスに投与すると抗炎症作用があることも知られています。以上のように、バイオ医薬品のシアル化は安全性と有効性に影響を与える可能性があり、規制機関はグリカンのより厳密なキャラクタリゼーションを要求しています。これはバイオ医薬品の品質に関するEMAガイドラインで強調されており、先行バイオ医薬品とバイオシミラーの両方で、広範囲にわたる最先端の特性評価試験が並行して実施されることが求められています(以下参照)。
(“EMA Revises Biosimilars Guideline on Quality Issues”in Hogan Lovells (ed) Focus on Regulation, posted on June 9, 2014 by Elisabethann Wright and Ciara Farrell. )