■ 方法と解析
スタンダードカーブは、サンプル希釈液にて1000 pg/ml-25 pg/mlで調製し、正常ヒト血漿の3ロット[異なる抗凝固剤(Na-クエン酸、Na-EDTAおよびNa-ヘパリン)で処理したもの]および3ロットのプールから作成しました。加えて、ヒトIFNαA2a低(30 pg/ml)、中(300 pg/ml)および高(800 pg/ml)濃度での添加試験を2つの異なるロットの正常ヒト血漿で調製しました。これら2ロットはプールで使用したロットからのものとは異なります。続いて、Human Interferon Alpha Serum Sample Multi-Subtype ELISAキット(品番:41110-1)にて提供されたプレート上にサンプル希釈液50µl、スタンダード50µlを添加しました。残りのステップは、キットプロトコルに従って実施しました。
別のアッセイでは、プールヒト血漿中の1000〜25 pg/mlからのスタンダードカーブと、サンプル希釈液で希釈した50%プールヒト血漿中の500〜12.5pg/mlからのスタンダードカーブを比較しました。このアッセイでは、プールヒト血漿中の各スタンダード(1000〜25 pg/ml)50µlをプレート上のサンプル希釈液50µlに加え、50%希釈プール血漿の場合は、スタンダード(500〜12.5 pg/ml)100µlを直接プレートに添加しました。
各アッセイ終了後、プレートをVmaxプレートリーダー(Molecular Devices Corporation, CA)で測定しました。(吸光度450nm)Y軸上に平均OD@ 450nmを、(曲線ごとに)X軸上にpg/mlの実濃度をプロットしました。曲線は、非線形4パラメータフィット(図1〜5)を用いて生成しました。カーブフィット式とデータポイントに対する平均OD値に基づいて、推定濃度(バックフィット濃度)を各データポイントに対して決定し、全データをSoftMax Proバージョン5(Molecular Devices Corporation, CA)を用いて分析しました。
図1-3 サンプル希釈液のみ、異なる凝固剤を用いた3つの異なるロットの未処理血漿、
異なる凝固剤を用いた3つの異なるロットをプールした未処理血漿からのスタンダードカーブ(1000-25 pg/ml)
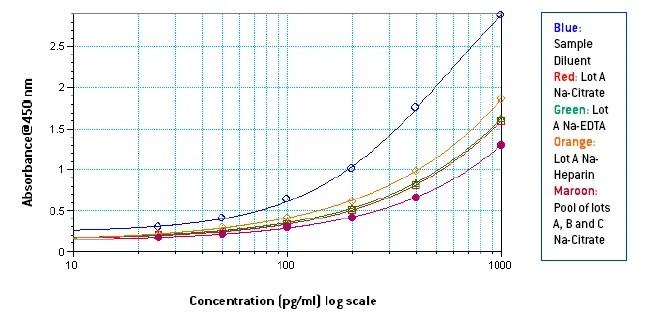
図1
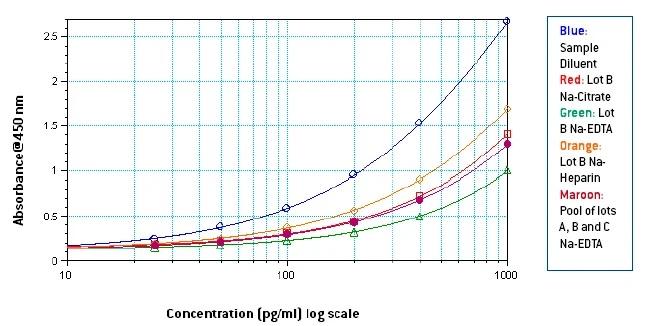
図2
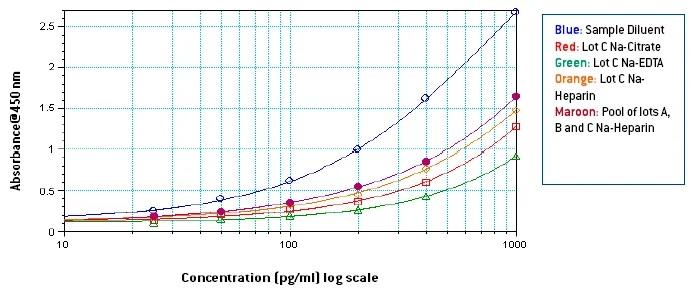
図3
図4-5:サンプル希釈液で調製した500-12.5 pg/mlのスタンダードカーブ、および50%希釈したプール血漿サンプルにおけるスタンダードカーブ(500-12.5 pg/ml)と
未処理血漿サンプルで調製したスタンダード(1000-25 pg/ml)をサンプル希釈液にて希釈し作成したスタンダードカーブ(500-12.5 pg/ml)との比較
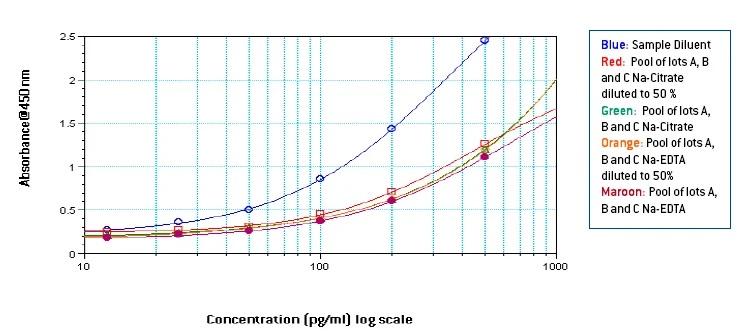
図4
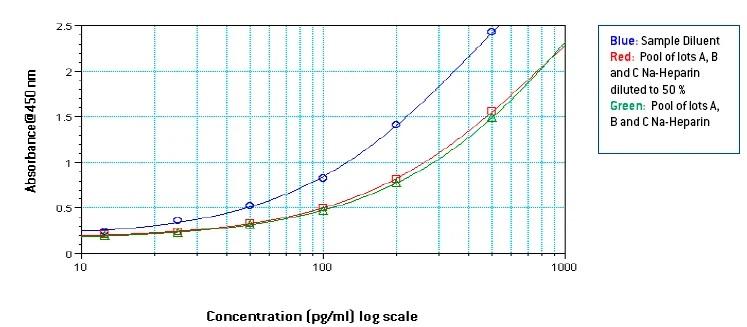
図5
表1 異なる抗凝固剤を用いたヒト血漿におけるヒトIFNαA2aの添加回収率(%)
| > Matrix |
30 pg/ml |
300 pg/ml |
800 pg/ml |
| Lot D with Na-Citrate |
61.2% |
102.2% |
91.5% |
| Lot E with Na-Citrate |
79.1% |
122.5% |
127.5% |
| Lot D with Na-EDTA |
60.6% |
84.7% |
76.81% |
| Lot E with Na-EDTA |
58.6% |
86.96% |
91.23% |
| Lot D with Na-Heparin |
91.88% |
107.68% |
94.88% |
| Lot E with Na-Heparin |
98.76% |
105.32% |
106.53% |
| Average |
75% |
101.56% |
98.1% |
図1-3から、Na-EDTAにおけるヒト血漿中のシグナルは、Na-クエン酸およびNa-ヘパリンにおけるヒト血漿中のシグナルよりも低いことが分かります。この作用はプール血漿でも同様に明らかです。Na-ヘパリン血漿におけるシグナルは3種類の抗凝固因子の中で最も強く、また、サンプル希釈液中のシグナルと比較して、血漿中の成分によるヒト血漿中のシグナルの抑制も明らかでした。
図4-5から、プレート上のIFNαの濃度に一致するOD値に基づいて、プレート上のサンプル希釈液50µlに非希釈プール血漿で調製した各スタンダード(1000〜25 pg/ml)50µlを添加したサンプルからのスタンダードカーブは、使用した抗凝固剤に関係なく50%希釈のプール血漿で調製した各スタンダード(500〜12.5 pg/ml)からのスタンダードカーブと類似していることが観察されました。しかし、異なるドナー由来の血漿中の成分量や個体差のために、2つの曲線間の類似性の程度は、血漿のロットごとに異なる可能性があります。
表1から、IFNαA2a(30 pg/ml)の低濃度添加における添加回収率は、Na-EDTAを含む血漿の場合に最も低く、Na-ヘパリンを含む血漿の場合に最も高いことが観察されます。 全体として、平均添加回収率は許容可能な業界標準の範囲内です。































