CD44v9 抗体/CD44v10-e16 抗体の使用例 がん幹細胞Cancer Stem Cell ;CSCs応用例
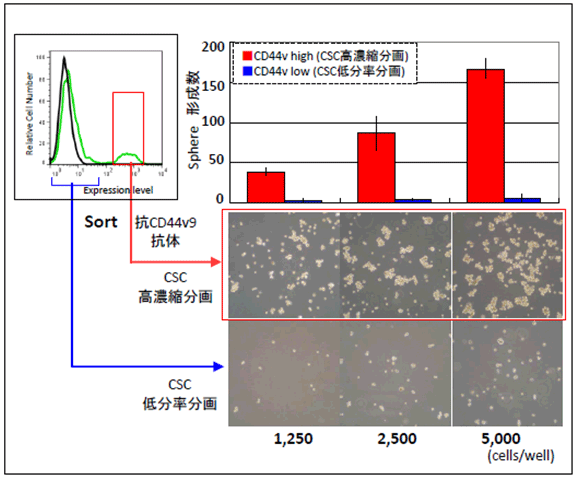
薬剤のがん幹細胞(CSC)への作用を評価する代表的なin vitro系としてSphere Formation Assayがあります。これは、がん幹細胞(CSC)の特性である腫瘍形成能を利用し、「培養系中に形成されるColony (スフィアと呼ばれる)数によりがん幹細胞(CSC)の数を定量する方法」で、これにより薬剤を作用した時のスフィア数の減少により、薬剤のがん幹細胞(CSC)への作用効果を定量する事が可能となります。
手順は、 がん幹細胞(CSC)の高濃縮群の細胞を103 細胞/ウェル程度の濃度で低吸着plateに播種・培養すると、下図の写真に示すように多数のスフィアが形成されます。これに対して薬剤を作用させた時の、形成スフィア数の減少を評価します。スフィア数の減少はがん幹細胞(CSC)の減少と相関する事から、これにより薬剤のがん幹細胞(CSC)への作用を定量的に評価する事ができます。
しかし、通常の細胞株または、CSC低分率分画群では、がん幹細胞(CSC)が希少量しか含まれず、殆どスフィアが形成されないため薬剤の効果を評価する事が困難です。
前立腺がん細胞株 PC-3 によるスフィア形成
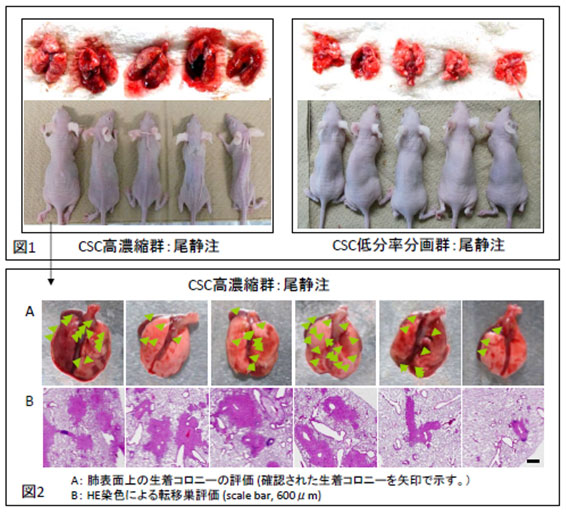
遠隔臓器における転移巣の形成能は、がん幹細胞(CSC)の保有する特性の1つです。
マウスにがん細胞を尾静注した場合、通常、含まれるがん幹細胞(CSC)が希少のため形成される転移巣は図1の右図のCSC低分率分画群の場合と同じように希少であり、薬剤の転移阻害、即ちがん幹細胞(CSC)への作用を有意に評価する事が困難です。
本抗体を用いて濃縮したCSC高濃縮細胞群を尾静注した場合、図1の左図に示すように、有意に多数の肺転移巣が形成され、薬剤投与時の効果を確認する事が可能となります。図2に、肺表面および内部に形成された転移巣の例を示します。
既に、この系を用いて、がん幹細胞の治療薬開発に成功した事例もあり、今後、がん幹細胞治療薬開発のための有力なツールとなる事が期待されます。
膵臓がん細胞株AsPC-1尾静注による転移巣形成能評価
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について























 このページを印刷する
このページを印刷する













