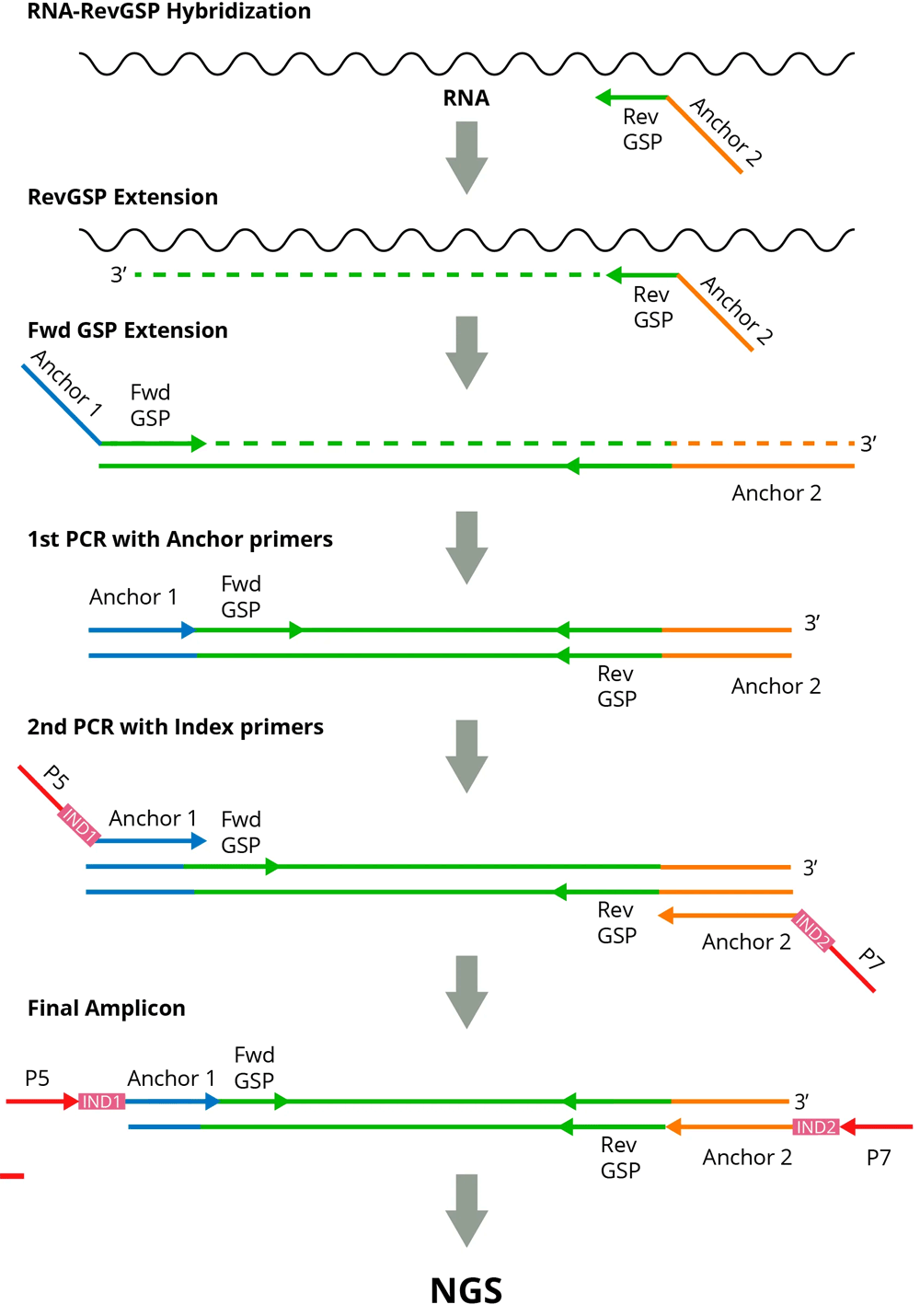
本商品は、マルチプレックスRT-PCRと次世代シーケンシング(NGS)のプロトコルを組み合わせた約19,000種類のヒト遺伝子の発現レベルを同時に解析することができるキットです。
最低 10 pg の total RNA から 19,000 種の遺伝子発現レベルを高感度に測定! DriverMap™ Expression (EXP) ヒトゲノムワイド発現プロファイリングキット
- カテゴリから探す > 分子生物 > DNAシーケンシング > 次世代シーケンシングキット
特長
- 最低10pg(single cell)のTotal RNAから解析可能
- RNA-seq解析と比較して約100倍高感度、105倍の検出範囲
- 特異性が高い検証済みプライマーを使用するため、低発現の遺伝子も検出可能
ワークフロー
プライマー検証
数千種類のPCRプライマーを実験的に検証し、19,000種類のヒト遺伝子および5,000種類のマウス遺伝子に対する対応するプライマーを設計しました。
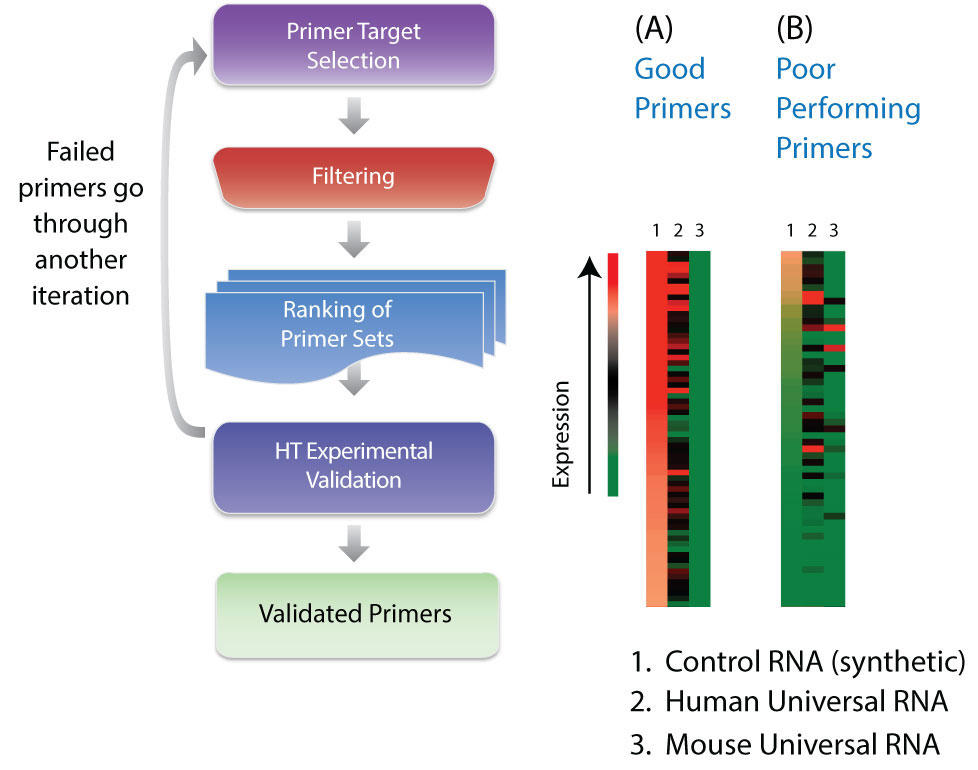
図2: プライマーの開発手順
複数回のマルチプレックスRT-PCR/NGS実験を連続的に行い、各遺伝子を標的とするPCRプライマーより、オンターゲット効果が高く、オフターゲット活性の低いプライマーを実験的に選択した。
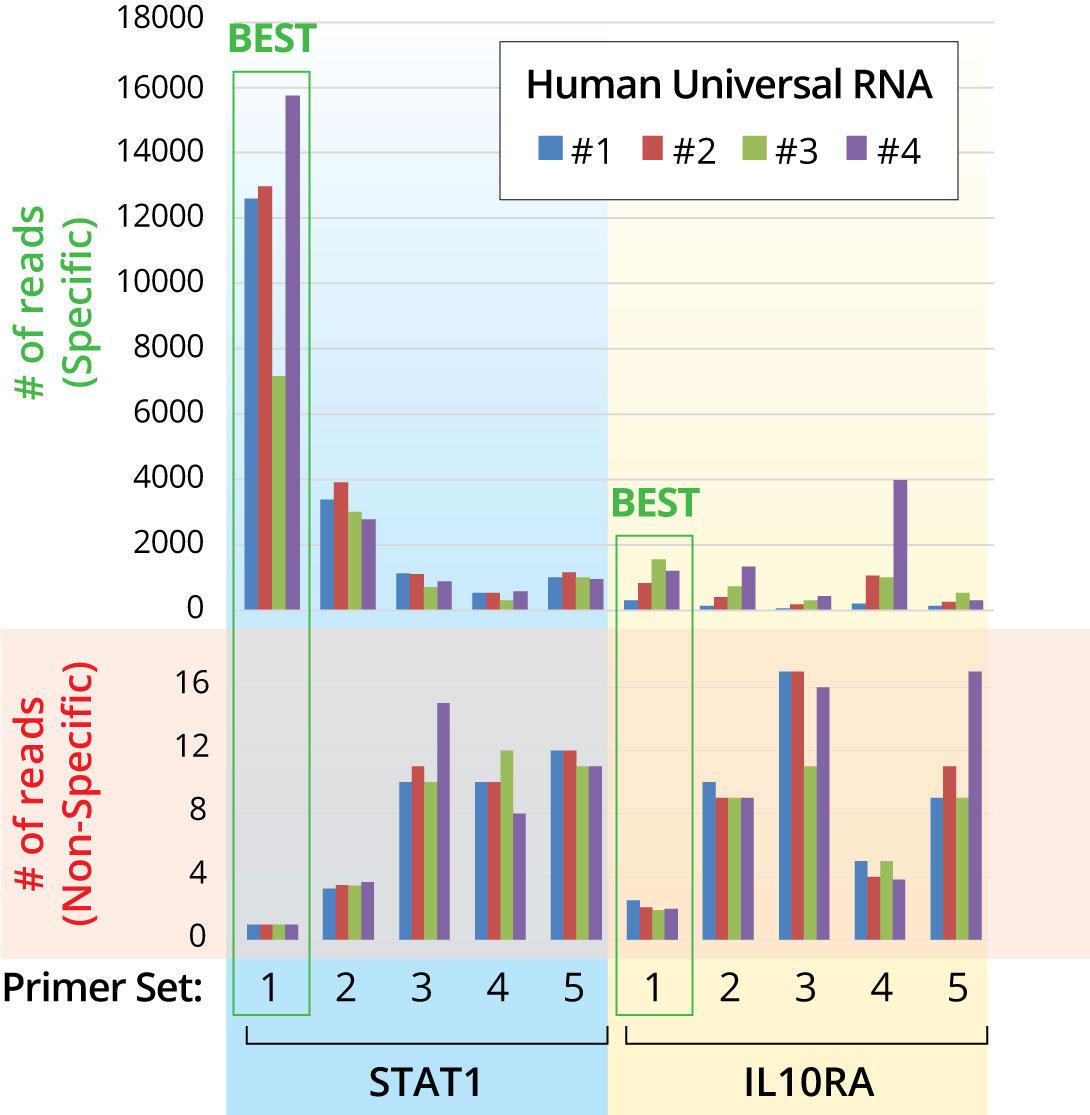
図3: プライマーの実験検証
各遺伝子について、mRNAアイソフォームの保存部分を標的とするプライマーを複数設計し、高効率、高感度、高特異性にプライマーを選択した。さらに、高発現の遺伝子についてはあえて特異性の低いプライマーを選択し、過剰なシーケンスを防いでいる。
データ例
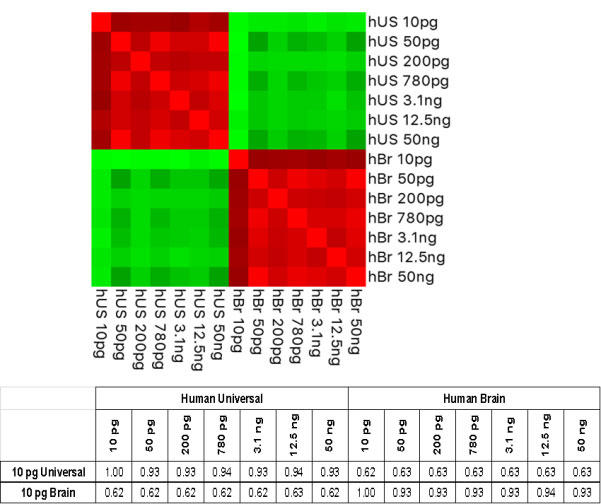
図4: 再現性が高い遺伝子検出
ヒトユニバーサルRNAと脳由来total RNA間において、検出された遺伝子の一貫性がみられ、再現性が高いことが示された。
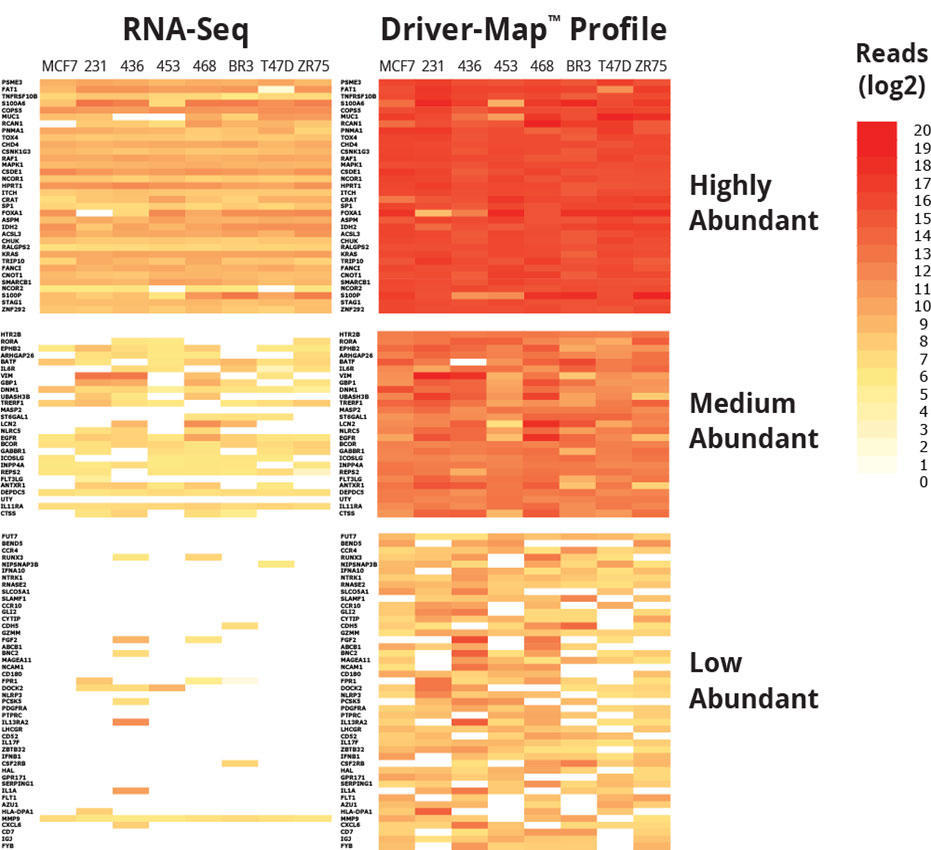
図5: RNA-Seq vs DriverMap™ Assay Heatmap
DriverMap™はRNA-Seqより100倍高感度であるため、低発現の遺伝子をより多く検出可能。また、RNA-seq よりも検出範囲が広く、高発現の遺伝子においても発現量に差のある場合はその差をよりよく検出可能。
アプリケーション例
- 全血サンプルからのバイオマーカー探索
rRNAやグロビン除去の必要なく全血由来 RNA (PAXgene 等) を使用可能 - 循環腫瘍細胞 (CTC) 分析
増幅工程が必要ありません - 腫瘍細胞構成解析
腫瘍/間質細胞の構成および浸潤性免疫細胞型を評価するための包括的発現プロファイル - 患者由来の異種移植(PDX)モデル
モデル動物のバックグラウンド細胞からヒト細胞を分離することなく、ヒト特異的発現プロファイルを取得可能 - 細胞株の発現解析
96ウェルまたは384ウェルの単一チューブプロトコルにより、化学的および遺伝的摂動メカニズムの同定が容易 - 希少で限られた細胞集団の発現プロファイリング
FACS、磁気ビーズまたはマイクロ流路、細針生検、およびレーザーキャプチャーマイクロダイセクションによって単離された少数細胞での包括的な分析
製品ラインアップ
ゲノムワイドの遺伝子を標的にしたキットに加え、癌および炎症性疾患、細胞シグナル伝達、細胞系統、分化および免疫活性化に関する遺伝子を特異的に増幅するパネルキットもラインアップしております。
| パネル | 遺伝子数 |
|---|---|
| Human Genome Wide | 19,000 |
| Human Cell Marker Panel | 1,285 |
| Human Hallmark Signatures Panel | 4304 |
| Human LINCSx Panel | 1,573 |
| Human Pan-Cancer Pathway Panel | 2,094 |
| Human Transcription Factor Signatures Panel | 2,649 |
| Mouse Targeted Panel | 4,700 |
希望販売価格
ゲノムワイド RNA 発現プロファイリング
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
| DriverMapTM EXP Human Genome-wide 19K Profiling Kit, V3 |
CLT | DM3-HGW-24 | 1 KIT [for 24 reactions] |
¥410,000 |
| DriverMapTM EXP Human Genome-wide 19K Profiling Kit, V3 |
CLT | DM3-HGW-96 | 1 KIT [for 96 reactions] |
お問い合わせ |
| DriverMapTMEXP Human Genome-wide 19K Dried Blood Microsamples Profiling Kit, V3 (24 multiplex) |
CLT | DM3-HGW-DB-24 | 1 KIT [for 24 reactions] |
¥430,000 |
| DriverMapTMEXP Human Genome-wide 19K Dried Blood Microsamples Profiling Kit, V3 (96 multiplex) |
CLT | DM3-HGW-DB-96 | 1 KIT [for 96 reactions] |
¥1,530,000 |
標的遺伝子発現プロファイリング
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
DriverMapTM Human Cell Marker Panel (96 multiplex)  |
CLT | DMF-HCM-96 | 1 KIT [for 96 reactions] |
¥800,000 |
DriverMapTM Human Hallmark Signatures Panel (96 multiplex)  |
CLT | DMF-HHM-96 | 1 KIT [for 96 reactions] |
¥800,000 |
DriverMapTM Human LINCSx Panel (96 multiplex)  |
CLT | DMF-HLX-96 | 1 KIT [for 96 reactions] |
¥800,000 |
DriverMapTM Human PanCancer Panel (96 multiplex)  |
CLT | DMF-HPC-96 | 1 KIT [for 96 reactions] |
¥800,000 |
DriverMapTM Human TransFactor Signatures Panel (96 multiplex)  |
CLT | DMF-HTF-96 | 1 KIT [for 96 reactions] |
¥800,000 |
DriverMapTM Mouse Targeted Panel (96 multiplex)  |
CLT | DMF-MPLH-96 | 1 KIT [for 96 reactions] |
¥800,000 |
| DriverMapTMMouse Targeted Panel |
CLT | DMF-MPLH-24 | 1 KIT [for 24 reactions] |
¥240,000 |
関連サービス
- Cellecta社 DriverMap™ 解析受託サービス
- 低発現のクロノタイプ検出に最適!TCR/BCRレパトア解析用キット
DriverMap™ Adaptive Immune Receptor (AIR) TCR-BCR プロファイリングキット - 簡便かつ低コスト!シングルセルTCR/BCRレパトア解析キット
DriverMap™ Single-Cell Adaptive Immune Receptor(AIR)TCR-BCR アッセイキット
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について
※ CAS Registry Numbers have not been verified by CAS and may be inaccurate.
- 「DriverMap™ Expression (EXP) ヒトゲノムワイド発現プロファイリングキット」は、下記のカテゴリーに属しています。
-
- カテゴリから探す > 分子生物 > DNAシーケンシング > 次世代シーケンシングキット























 このページを印刷する
このページを印刷する