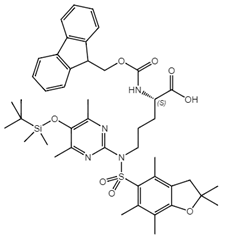
Argpyrimidine はメイラード反応のような非酵素的な翻訳後修飾の結果起こります。この変化が機能や安定性に及ぼす影響を調べるにはビルディングブロックが必要です。

翻訳後修飾(post-translational protein modification:PTM)は、自然界に広く存在し、ほとんどの場合、生体にとって望ましい修飾です。一般的に、これらの修飾は、リン酸化、グリコシル化、ファルネシル化など、酵素を介した標的化です。
しかし、タンパク質が受ける非酵素的修飾(non-enzymatic modifications:nPTM)も存在します。老化、糖尿病や癌などの様々な疾患により、あるいは熱への暴露などを介して行われる修飾です。この修飾は代謝性化合物との不要な反応である場合が多いです。例えば、表面に露出したリジンやアルギニンの側鎖は、代謝物であるメチルグリオキサールと反応し、最終的にカルボキシエチルリジン(CEL)、メチルグリオキサール-ヒドロイミダゾロン(MG-H1)、Argpyrimidine(Apy)などを生成します。
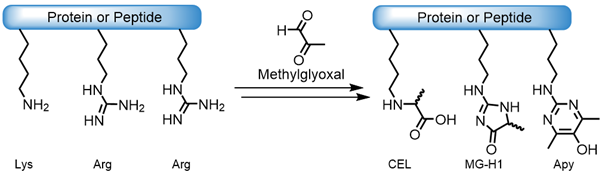
図. 表面露出したLys-/Arg側鎖とメチルグリオキサールとの反応
Apyは、老化や白内障の眼球レンズ、アミロイドポリニューロパチー患者のアミロイド線維、糖尿病患者やがん患者の細胞や組織から検出されています。このようなApy形成による生物学的影響の解明には、目的とするペプチドやタンパク質に決められた位置へ定量的にArgpyrimidineを導入することが重要になってきます。これは、固相ペプチド合成 (solid phase peptide synthesis:SPPS) により形成することが可能です。一般的なSPPS条件下で実施するには、α-アミンのFmoc保護と酸に親和性のある保護基による側鎖保護がされた Amyビルディングブロックが必要です。
側鎖保護基の組み合わせは、一般的なFmoc合成条件に対して直交性という条件を満たすだけでなく、合理的な収率で合成可能なものでなければなりません。ウィーン大学 Christian F. W. Becker教授とそのチームは、試行錯誤を重ねた結果、ビルディングブロックであるFmoc-Argpyrimidine (Pbf,TBMS)-OH (FAA5530) を開発しました。このビルディングブロックは標準SPPSプロトコルで簡単に使用でき、Iris Biotechから販売しています。より大きなタンパク質にArgpyrimidineを導入するためには、半合成的なアプローチが可能です。
- タンパク質の最も大きな部分を組換え合成で生産する。
- Apyを含むフラグメントをSPPS化する。
- フラグメントを最終的な全長タンパク質に縮合する。
非酵素的翻訳後修飾(nPTM)を施したタンパク質の製造方法という興味深い旅についてもっと知りたい方は、ベッカー教授のワークショップ![]() に参加してみてはいかがでしょうか。
に参加してみてはいかがでしょうか。
この種の修飾アミノ酸は、遊離アミノ酸として、あるいは質量分析用に重水素で標識したもの、SPPS用に多面的に保護したビルディングブロックとして、「メイラード反応産物」に掲載されています。























 このページを印刷する
このページを印刷する