|
吉本 尚平 先生 福岡歯科大学 病態構造学分野 |
Genocel® パウダータイプを用いたスフェロイド培養
ユーザーレポート
Product
メーカー:株式会社ニッケ・メディカル メーカー略号:NIK

■ 細胞培養用ゼラチン繊維基材 Genocel®
独自の不織布構造のゼラチンを用いた、細胞培養用基材です。強度が高く、容易に細胞培養を行うことができます。
シートタイプ(5 mm、8 mm)、ブロックタイプ(4 mm)、パウダータイプの3種類をご用意しています。
パウダータイプの特長
- 生体適合性に優れるゼラチンの繊維パウダー
- 栄養・酸素の透過性の高いゼラチンハイドロゲル
- 培地に混ぜて加えるだけで、細胞活性が向上
- 3次元構造体の作製時に加えると機械強度が向上
実験内容
培養細胞株を用いた実験は、簡便で、再現性も高いことから、生命科学分野における基本的な実験手法の一つとなっています。しかし、プラスチックプレート上での平面的な細胞培養は、観察対象の分子によっては、生体内での状態と乖離していることがわかってきました。そのため、より生体に近い実験系を構築するために、三次元的な培養が広く行われるようになってきています。
細胞株を用いた三次元の培養系でもっとも簡便なのが、スフェロイド培養です。非接着処理がなされたUボトムプレート等を用いて細胞塊を作り培養する手法で、プレートに細胞を播種するだけで、時間経過とともに細胞の凝集体が形成されます。しかし、細胞の種類によって、特に細胞間接着の強い上皮系の細胞株では、スフェロイドを大きくしたり(播種細胞数の増加)、培養期間を長く設定したりすることにより、スフェロイド中心部での細胞死が起こりやすくなってしまいます。
このような問題の解決策の一つとして、今回、Genocel® パウダータイプを用いたスフェロイド培養を行いました。Genocel®は生体適合性に優れるゼラチンの繊維パウダーで、栄養・酸素の透過性の高いゼラチンハイドロゲルにより構成されています。パウダー状のため、任意の分量を培地に添加しスフェロイド培養の基材として使用することできます。Genocel® パウダータイプを添加しスフェロイドを作製することで、スフェロイド中心部まで細胞死の起こりにくい状態での培養が可能となりました。また、スフェロイドサイズの向上が図れ、培養後の染色やその他アッセイ時のハンドリングの良さも感じられました。
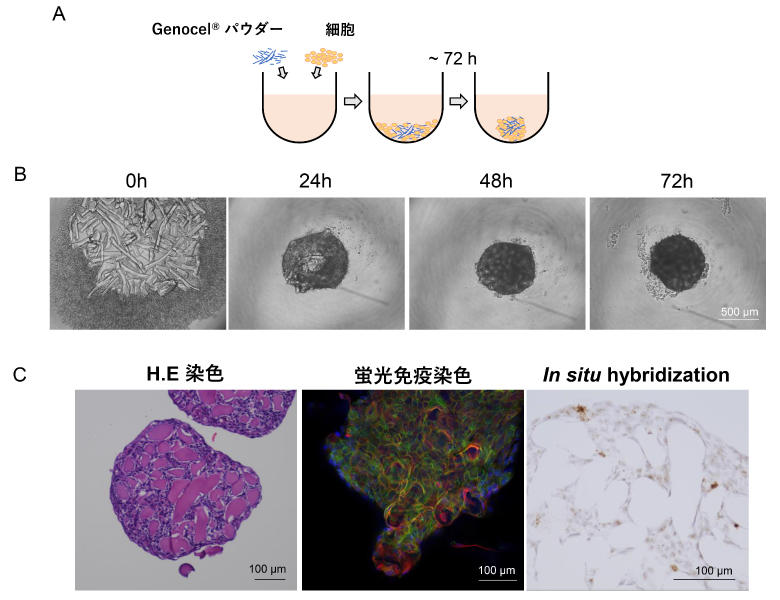
以下に簡単な実験手順をあげます。(図A、B)
- 培地にGenocel® パウダータイプを添加したもの(パウダー懸濁培地:0.1 mg/ml)をスフェロイド作製用の96ウェルプレートにパウダーが0.01 mg/wellとなるように分け入れる。
この際、パウダー量が均等になっているかを顕微鏡で確認すると、大きさのそろったスフェロイドが作成できます。 - スフェロイドとする細胞の懸濁液を1×104 cell/wellとなるように各ウェルに播種する。
- 37℃、5% CO2 でインキュベートし経時的に観察を行う。培地の交換は半量を目安に適宜行う。
- 各種アッセイに用いる。染色実験の場合はピペットで回収して任意の固定液で固定を行う。
パウダー量、細胞数を調整することで、任意の大きさのスフェロイドの作製が可能でした。また、スフェロイド形成後に薬剤刺激を行う等、比較的長い培養期間が必要な実験においても中心部の細胞死を起こすことなく実験が可能でした。また、スフェロイドのサイズを大きくすることで、ホルマリン固定パラフィン包埋(FFPE)切片の作製や凍結切片の作製も容易に行うことができました。もちろん、切片にすることなくスフェロイドのまま(適宜、透明化処理等をおこなって)蛍光免疫染色を行うことも可能です(図C)。
このように、Genocel® パウダータイプを用いて、内部まで細胞活性の保たれたスフェロイドを簡便に作ることできます。これにより、スフェロイド実験を単純な形成率やサイズの評価のみならず、免疫染色でのタンパク発現解析やin situハイブリダイゼーションでのRNA発現解析にも応用することができ、実験の幅が飛躍的に広がりました。
我々の使用経験から、スフェロイド培養におけるGenocel® パウダータイプの有用性を紹介させていただきました。このノートが研究者の皆様のお役に立てればと思います。
- Shohei Yoshimoto, Hiromitsu Morita, Kazuhiko Okamura, Akimitsu Hiraki, Shuichi Hashimoto,et. al αTAT1-induced tubulin acetylation promotes ameloblastoma migration and invasion Lab Invest. 2022, 102 (1):80-89.
























 このページを印刷する
このページを印刷する