抗CTLA-4抗体の投与とネオアンチゲンDNAワクチン(C20)による免疫を併用した群では、すべてのマウスにおいて100%の腫瘍退縮が認められ、その後250日以上にわたり腫瘍の再発は確認されませんでした(図1b)。
ネオアンチゲン特異的T細胞は、ネオアンチゲンDNAワクチン(C20)を投与したマウスおよび抗CTLA-4抗体を投与したマウスのいずれにおいても、腫瘍組織および脾臓の両方で統計的に有意な増加が認められました。一方で、抗PD-1抗体では同様の増加は認められませんでした(図1c)。
CTLA-4は制御性T細胞で発現することが知られており、抗CTLA-4抗体はこの細胞集団を減少させることが報告されています。本実験条件下では、ネオアンチゲン特異的CD8+T細胞 / 制御性T細胞の比率の有意な増加が確認されました(図1d)。
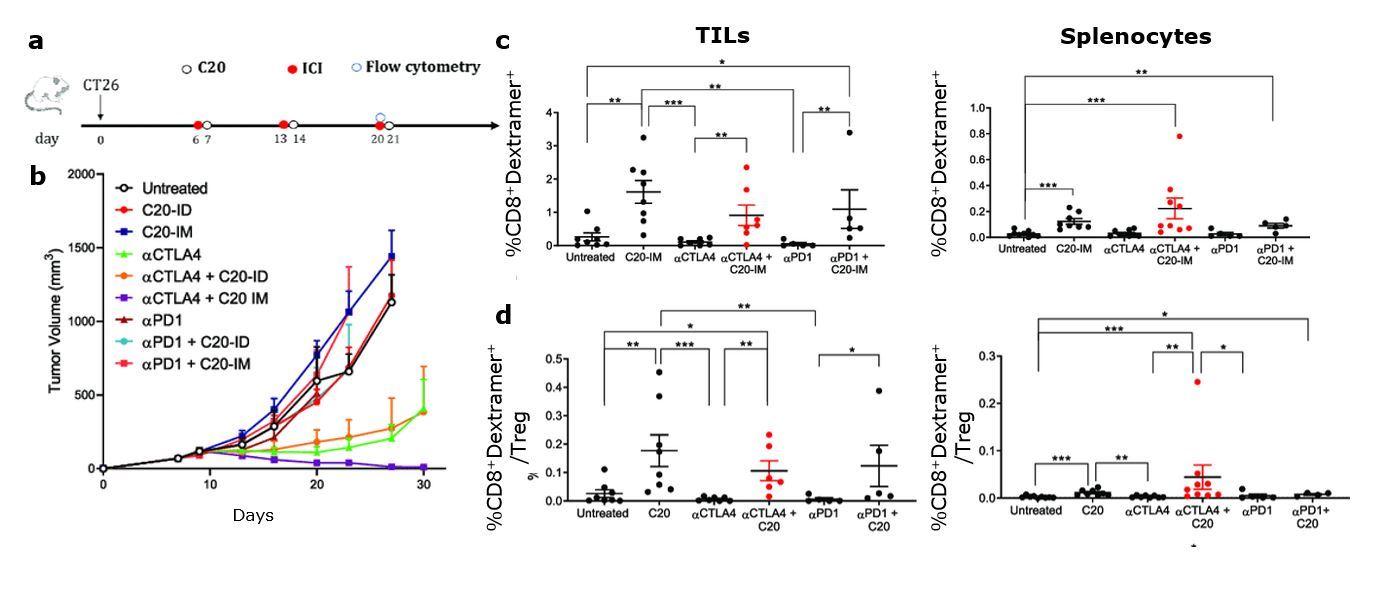
図1:抗CTLA-4抗体とネオアンチゲンDNAワクチン(C20)併用治療による治療効果およびネオアンチゲン特異的免疫応答
a)抗CTLA-4抗体とC20ワクチンを併用した治療スケジュール
b)腫瘍体積の測定結果
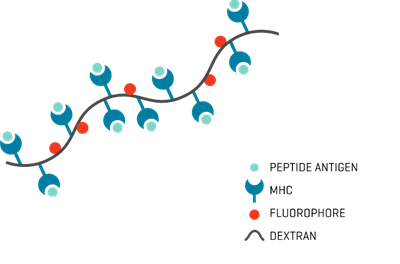
c)MHC Dextramer®(H-2Dd/SGPSYATYL)を用い、生細胞中のCD45+ CD3+ CD8+細胞をゲーティングして測定したネオアンチゲン特異的T細胞応答の頻度
d)生細胞中のCD45+ CD3+ CD4+細胞をゲーティングして評価した制御性T細胞集団を、Dextramer®陽性細胞との比として表示
IM: 筋肉注射, ID: 皮内注射