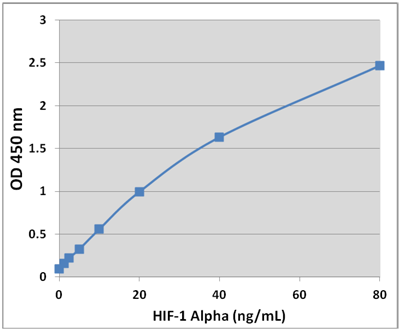
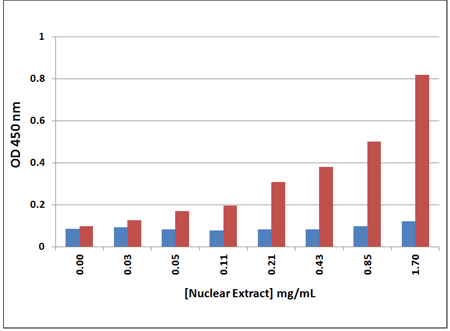
HIF-1α とは
哺乳動物細胞は、低酸素状態の感知することができ、低酸素応答性の一連の遺伝子をオンにします。
低酸素誘導因子 HIF-1(hypoxia-inducible factor 1)は、VEGFやエリスロポエチン(erythropoietin)を含むいくつかの低酸素応答性遺伝子の活性化に関与します。HIF-1複合体は、HIF-1b/ARNT とHIF-1 Alpha(HIF-1α)の2つのタンパク質サブユニットから構成されます。HIF-1α は、正常な酸素条件下では継続的にユビキチンプロテアソーム系(UPS)によって分解されるため、検出されません。一方、低酸素条件下では、HIF-1α は安定化・蓄積し、細胞質から核へ移行後にHIF-1b/ARNTと二量体化して転写活性を示します。HIF-1複合体は、低酸素応答性領域(HREs:hypoxic response elements)に作用し、遺伝子発現を誘導する転写コアクチベーターを結合します。HIF-1 の安定性と機能の厳格な制御は、翻訳後修飾(ヒドロキシル化、ユビキチン化、アセチル化、およびリン酸化など)によって調整されます。
通常の酸素条件下においてHIF-1αの翻訳後修飾は、N末端トランス活性化領域、C末端トランス活性化領域、酸素依存的分解領域(ODDD:oxygen dependent degradation domain)で発生します。2つのプロリン残基のヒドロキシル化およびODDD中リジン残基のアセチル化は、HIF-1と von Hippel-Lindau (pVHL) ubiquitin E3 ligase complexの結合を促進します。pVHL complexはHIF-1をユビキチン化修飾し、26Sプロテアソームによって分解します。また、C末端トランス活性化領域中のC末端のアスパラギン残基のヒドロキシル化は、HIF-1とCBP/p300 との相互作用をブロックするため、HIF-1 転写活性が阻害されます。HIF-1αが合成されると、2-オキソグルタル酸ジオキシゲナーゼによって402番目と564番目のプロリン残基が急速にヒドロキシル化されます。これらのジオキシゲナーゼ(proline hydroxylase domains (PHDs))が低酸素または化学的に不活性化されると、HIF-1αの半減期が増加し、続く複合体の活性化をもたらします。























 このページを印刷する
このページを印刷する