2022年のノーベル化学賞はバリー・シャープレス氏,モーテン・メルダル氏およびキャロライン・ベルトッツィ氏によるクリックケミストリー(Click Chemistry)の研究業績に授与されることが決定しました 。
2022年のノーベル化学賞はバリー・シャープレス氏,モーテン・メルダル氏およびキャロライン・ベルトッツィ氏によるクリックケミストリー(Click Chemistry)の研究業績に授与されることが決定しました 。
第一世代のクリックケミストリー:CuAAC
20世紀の変わり目頃、バリー・シャープレス氏は、ビルディングブロックが「簡単に」はまり合うような化学的変換の一種を研究していました。バリー・シャープレス氏とモーテン・メルダル氏は、互いに独立して、「クリックケミストリー」と呼ばれる、銅触媒によるアジド-アルキン1,3-双極子環状付加反応を発見しました。この反応は、さまざまな分野で幅広い応用性があり、現在最も広く使用されている結合技術です。銅触媒によるアジド-アルキン環化付加により、1,4-二置換異性体が得られます。
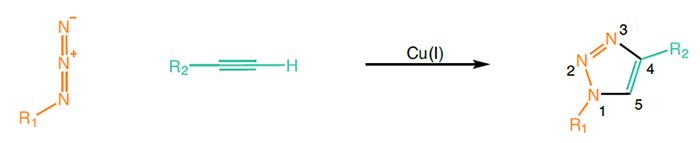
図1:銅触媒によるアジド-アルキン環化付加反応により、1,4-二置換トリアゾールが得られる。
注目すべきは、ルテニウムがアジドとアルキンの間の 1,3-双極子環状付加を触媒して、代わりに 1,5-二置換位置異性体を生成することもできるという事実です。 しかしながら、銅の存在は、高い細胞毒性、タンパク質の望ましくない酸化、ナノ結晶の発光特性の阻害などのいくつかの理由により、この反応のin vivoでのアプリケーションを制限してしまいます。
第二世代のクリックケミストリー:SPAAC
その後、キャロライン・ベルトッツィ氏により、クリック技術は新たな次元に推し進められ、正常な細胞機能を妨げることなく生体に適合するクリック反応(=生体直交型クリック反応:bioorthogonal Click reactions)が開発されました。 いわゆる銅を含まないひずみ促進型アジド-アルキン環化付加(strain-promoted azide-alkyne cycloaddition:SPAAC)は、銅を含まないクリック反応として、幅広い研究分野で広く利用されています。しかしながら、シクロオクチンを使用する場合には、その高い反応性に加えて、保存中及び実験中に熱分解および(または)オリゴマー化を引き起こすという欠点もあります。さらに、タンパク質やペプチドのシステイン残基などの生体分子内チオールと競合的に起こる付加反応は、それらの生体直交性を弱めることになり得ます。
一方で、比較的新しく開発された4,8-diazacyclononynes(DACN)は、高い熱的及び化学的安定性を有し、高い反応性と親水性を示し、さらにynophilesに対する高い選択性も示します。
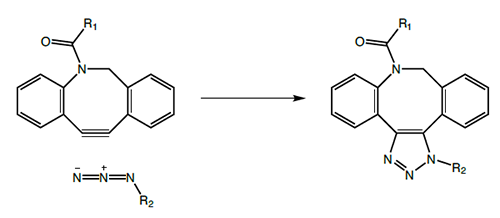
図2:SPAACの概略図
第三世代のクリックケミストリー:IEDDA
テトラジンライゲーションは、銅を含まない、迅速かつ完全な生体直交性型のクリックケミストリーの選択肢を提供することができます。機構的には、この反応はテトラジンとトランス-シクロオクテン(TCO)、シクロプロパンまたはノルボルネン等の歪みアルキンとの間のinverse electron-demand Diels-Alder環状付加反応を介して進行します。続いて二窒素の脱離下でretro-Diels-Alder反応が進行し、この反応は不可逆的になります。その他の利点として、この反応は非常に低濃度で反応性に優れており、水系溶媒中で行うことができます。
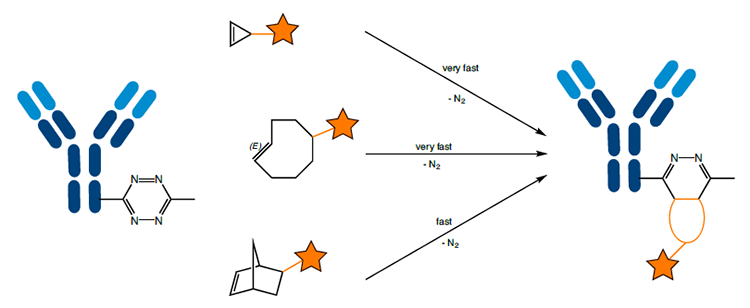
図3:テトラジンの一般的な反応パートナー
広く用いられているテトラジンには、主に6-メチル置換テトラジン(MeTz)と6-水素置換テトラジン(HTz)の2種類があります。MeTzは高い安定性を示すとともに、TCO誘導体との反応速度論が他の生体直交型反応ペアよりも速い(約1000M-1s-1)ことが知られています。HTzは、苛酷な反応条件に対しては安定性および耐性が低いですが、in vivoイメージングのような用途ではより速い反応速度(最大30000M-1s-1)を示します。
現在、クリックコンジュゲーションの技術の応用は、イメージングや創薬設計からセンサーの開発まで多岐にわたり、ケミカルバイオロジー、材料科学、表面化学、高分子化学など多様な分野に及んでいます。
Cosmo Bio would like to acknowledge and thank the Iris Biotech GmbH, Inc. for providing Click Chemistry information presented here.
- A Stepwise Huisgen Cycloaddition Process: Copper(I)-Catalyzed Regioselective “Ligation” of Azides and Terminal Alkynes; V. V. Rostovtsev, L. G. Green, V. V. Fokin, K. B. Sharpless; Angew. Chem. Int. Ed. 2002; 41: 2596-2599. https://doi.org/10.1002/1521-3773(20020715)41:143.0.Co;2-4
- CuI-Catalyzed Alkyne-Azide “Click” Cycloadditions from a Mechanistic and Synthetic Perspective; V. D. Bock, H. Hiemstra, J. H. van Maarseveen; Eur. J. Org. Chem. 2006; 2006: 51-68. https://doi.org/10.1002/ejoc.200500483
- A strain-promoted [3 + 2] azide-alkyne cycloaddition for covalent modification of biomolecules in living systems; N. J. Agard, J. A. Prescher, C. R. Bertozzi; J Am Chem Soc 2004; 126: 15046-7. https://doi.org/10.1021/ja044996f
- Bioconjugation with strained alkenes and alkynes; M. F. Debets, S. S. van Berkel, J. Dommerholt, A. T. Dirks, F. P. Rutjes, F. L. van Delft; Acc Chem Res 2011; 44: 805-15. https://doi.org/10.1021/ar200059z
- Strain-Promoted 1,3-Dipolar Cycloaddition of Cycloalkynes and Organic Azides; J. Dommerholt, F. Rutjes, F. L. van Delft; Top Curr Chem (Cham) 2016; 374: 16. https://doi.org/10.1007/s41061-016-0016-4
- Heteroatom-embedded Medium-Sized Cycloalkynes: Concise Synthesis, Structural Analysis, and Reactions; R. Ni, N. Mitsuda, T. Kashiwagi, K. Igawa, K. Tomooka; Angew. Chem. Int. Ed. 2015; 54: 1190-1194. https://doi.org/10.1002/anie.201409910
- Biomedical applications of tetrazine cycloadditions; N. K. Devaraj, R. Weissleder; Acc Chem Res 2011; 44: 816-27. https://doi.org/10.1021/ar200037t
- Inverse electron demand Diels-Alder (iEDDA)-initiated conjugation: a (high) potential click chemistry scheme; A. C. Knall, C. Slugovc; Chem Soc Rev 2013; 42: 5131-42. https://doi.org/10.1039/c3cs60049a
- Highly accelerated inverse electron-demand cycloaddition of electron-deficient azides with aliphatic cyclooctynes; J. Dommerholt, O. van Rooijen, A. Borrmann, C. F. Guerra, F. M. Bickelhaupt, F. L. van Delft; Nat Commun 2014; 5: 5378. https://doi.org/10.1038/ncomms6378
- Inverse electron demand Diels-Alder (IEDDA) reactions in peptide chemistry; M. Pagel; J. Pept. Sci. 2019; 25: e3141. https://doi.org/10.1002/psc.3141
- Tetrazine-Based Cycloadditions: Application to Pretargeted Live Cell Imaging; N. K. Devaraj, R. Weissleder, S. A. Hilderbrand; Bioconjug. Chem. 2008; 19: 2297-2299. https://doi.org/10.1021/bc8004446
- https://www.nobelprize.org/prizes/chemistry/2022/popular-information/?amp;amp [17.10.2022]























 このページを印刷する
このページを印刷する IRIS社
IRIS社