血液サンプルや細胞培養上清からエクソソームを直接定量! CD9 / CD63 ELISA キット (ヒト由来エクソソーム定量用)
背景
エクソソームは生体を構成するほぼすべての細胞から分泌される直径 30〜200 nm の小胞で、血液や尿などあらゆる体液中に存在します(1)〜(5)。また、in vitro では動物細胞の培養上清にも分泌されます。エクソソームは細胞と同様に脂質二重膜に包まれており、その表面には膜タンパク質が存在し、内部にはタンパク質やマイクロRNA などが包含されています。エクソソームを取り込んだ標的細胞において、これらのタンパク質やマイクロRNA が機能することによって、エクソソームは細胞間のコミュニケーションを担っていると考えられます(6)。エクソソームの構造上の特徴の一つとしてその表面に存在するテトラスパニンファミリーがあげられます。CD9 やCD63 はそのメンバー分子で、エクソソームの表面マーカーでもあります(7)。
エクソソームの定量法としては、エクソソームが内包するタンパク質量で代替する、あるいはナノトラッキング法による粒子解析などがありますが(8)、これらの方法は超遠心法などで一旦エクソソームを精製する必要があります。体液中や細胞培養上清中のエクソソームを直接定量する手段は極めて限られており、これまで一般的な方法は開発されてきませんでした。
本商品は、エクソソーム・マーカーである CD9 と CD63 に対する高性能抗体を用いたサンドイッチELISA により、体液中や細胞培養上清中に含まれる表面に CD9 分子と CD63 分子を合わせ持つエクソソームを相対的に定量することができます。
特長
- 血液サンプルや細胞培養上清などに含まれるヒト由来エクソソームを直接定量可能
- 感度:3.125 pg/mL、測定範囲:3.125〜200 pg/ mL
- 特殊な装置は不要で、通常のプレートリーダーがあれば測定可能(波長:450 nm)
- 標準試薬として保存安定性に欠けるエクソソームそのものを使用せず、CD9/CD63 融合タンパク質(標準タンパク質)を 利用することで安定性と再現性を確保
- CD9/CD63 融合タンパク質(標準タンパク質)で補正することで各サンプルの相対定量が可能
- 固相化した CD9 抗体 (12A12) でエクソソームを捕捉し、HRP 標識した CD63 抗体(8A12)で検出
構成内容
- 抗CD9 抗体固相化 96 ウェルプレート
- 標準タンパク質(2,000 pg/mL)
- アッセイバッファー
- 洗浄バッファー(10X )
- HRP 標識抗CD63 抗体(500X)
- 基質液
- 停止液(2N H2SO4)
- プレートシール
製品データ
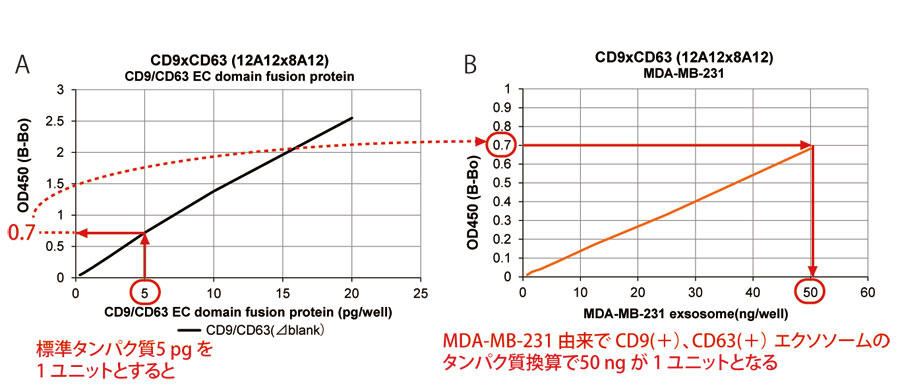
標準タンパク質による標準化と相対定量の概要
CD9/CD63 融合タンパク質を標準タンパク質として検量線を描き(図1. A)、例えば CD9/CD63 融合タンパク質 5 pg を 1 ユニットと した場合、その OD450 測定値は約 0.7 です。MDA-MB-231 細胞由来エクソソームのOD450 測定値をプロットした図1. B に照合すると、 測定値が 0.7 に相当するのは、約 50 ng であり、これを CD9 陽性かつ CD63 陽性エクソソームとみなすことができます。このようにして、 異なるサンプル間、あるいは異なる実験間でもアッセイごとに CD9/CD63 融合タンパク質を使用した標準曲線で補正することで検体 中のエクソソーム量を直接比較することが可能となります。
ヒト血清 希釈直線性試験 および 添加回収試験
CD9/CD63 融合タンパク質(標準タンパク質)およびエクソソーム(超遠心法で回収)にヒト血清を添加して希釈系列を作成し、直線性が確保できるか検討しました。100 µL の ELISA 反応に対して血清 25 µL を添加して測定していますが、バッファー系の標準曲線と同様に希釈直線性が保たれています。
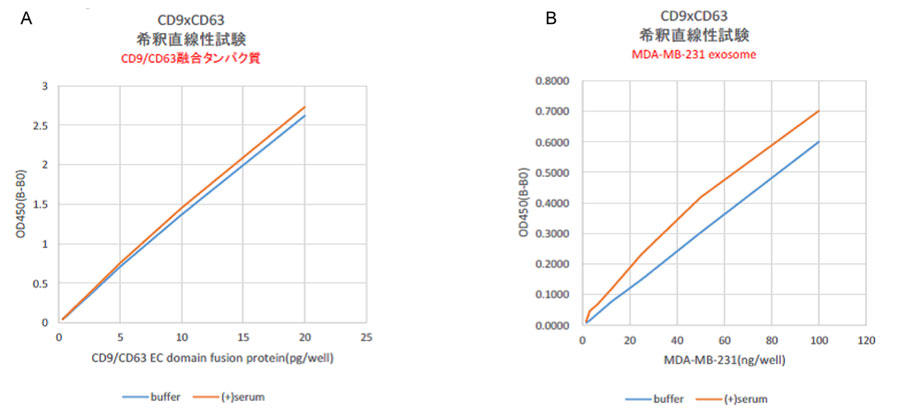
図2. 希釈直線性試験
ウェルあたりの血清添加量:25 µL
A:CD9/CD63 融合タンパク質(標準タンパク質)添加量:20 pg、 B:MDA-MB-231細胞由来エクソソーム添加量:100ng
CD9/CD63 融合タンパク質(標準タンパク質)および、MDA-MB-231 細胞由来エクソソームにヒト血清を添加し、2 倍ずつ段階希釈した場合もバッファー系の標準曲線と同様の直線性を示した。
次に、ヒト血清存在下において、CD9/CD63 融合タンパク質(標準タンパク質)、あるいはエクソソーム(超遠心法で回収)を添加した場合、どの程度の確率で添加量を回収できるか検討しました。CD9/CD63 融合タンパク質(標準タンパク質)は、20 µL/wellの血清存在下でも100%前後の添加回収率を示し、エクソソームではバラつきが生じたもののCD9/CD63 融合タンパク質(標準タンパク質)に準ずる結果が得られました。 希釈直線性試験結果と併せて、血清添加量25 µLまでの場合本アッセイ系における血清成分の影響は少ないと考えられます。
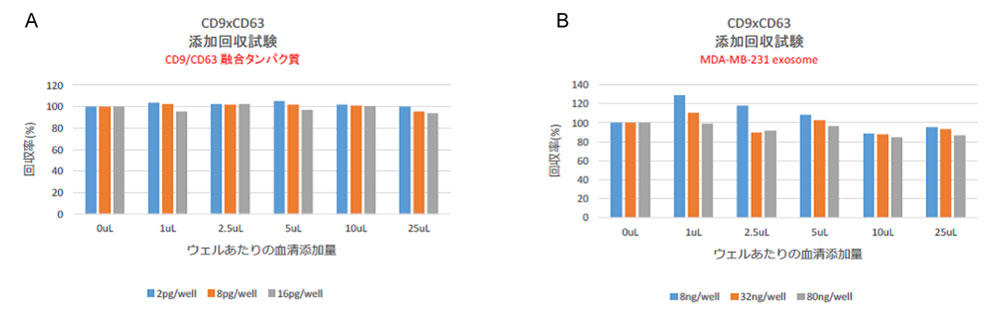
図3. 添加回収試験
ウェルあたりの血清添加量:1, 2.5, 5, 10, 25 µL
A:ウェルあたりのCD9/CD63 融合タンパク質(標準タンパク質)添加量:2, 8, 16 pg、B:ウェルあたりの MDA-MB-231 細胞由来エクソソーム添加量:8, 32, 80 ng
CD9/CD63 融合タンパク質(標準タンパク質)では、1ウェルあたり25 µLの血清存在下にといても100%前後の添加回収率を示し、MDA-MB-231細胞由来エクソソームにおいてもバラつきが生じたものの概ねCD9/CD63 融合タンパク質(標準タンパク質)に準ずる結果が得られた。
- [製品データ] 添加回収試験 測定値

細胞培養上清サンプルの測定
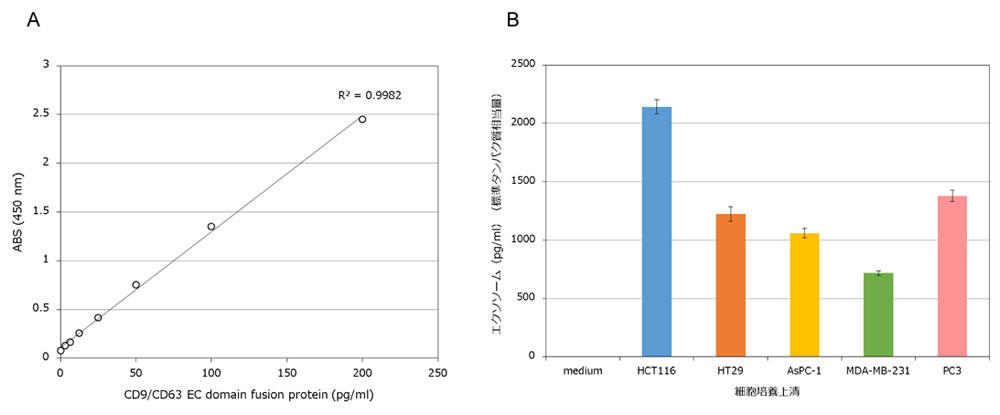
10% ウシ胎児血清 (FBS) を含む培地を用いて様々な細胞株 (HCT116、HT29、AsPC-1、MDA-MB-231、PC3)を8日間培養した後、遠心上清をサンプルとしました。測定値が検量線範囲内に収まるように適宜希釈し、希釈調整したCD9/CD63 融合タンパク質(標準タンパク質)とともに測定しました。 本アッセイでは、CD9/CD63 融合タンパク質(標準タンパク質)を基準とした相対定量を行います。CD9/CD63 融合タンパク質(標準タンパク質)の測定結果をもとに横軸に標準タンパク質量、縦軸に吸光度を取り検量線を描きます(図4.A )。この検量線とサンプルの吸光度を照らし合わせることで、サンプル中のエクソソーム量を標準タンパク質相当量として計算します(図4.B )。実験ごとに検量線を描くことで、異なる実験間のエクソソーム量を直接比較できます。
- J. Skog, T. Wurdinger, S. van Rijn, D. H. Meijer, L. Gainche, M. Sena-Esteves, W. T. Jr. Curry, B. S. Carter, A. M. Krichevsky and X. O. Breakefield: Nat Cell Biol., 10, 1470 (2008).
- T. Pisitkun, R. F. Shen and M. A. Knepper: Proc Natl Acad Sci USA., 101, 13368 (2004).
- S. Runz, S. Keller, C. Rupp, A. Stoeck, Y. Issa, D. Koensgen, A. Mustea, J. Sehouli, G. Kristiansen and P. Altevogt: Gynecol Oncol., 107, 563 (2007).
- S. Keller, A. K. Konig, F. Marme, S. Runz, S. Wolterink, D. Koensgen, A. Mustea, J. Sehouli and P. Altevogt: Cancer Lett., 278, 73 (2009).
- C. Lasser, V. Seyed AlikhS. Gabrielsson, J. Lotvall and H. Valadi: J Transl Med., 9, 9 (2011).
- Y. Naito, Y. Yoshioka, Y. Yamamoto and T. Ochiya: Cell Mol Life Sci., 74, 697 (2017).
- A. Zoraida and M. Yáñez-Mó: Front Immunol., 5, 442 (2014).
- V. Filipe, A. Hawe and W. Jiskoot: Pharm Res., 27, 796 (2010).
CD9 / CD63 ELISA キット (ヒト由来エクソソーム定量用)
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
| ヒト由来エクソソーム定量用 CD9×CD63 ELISAキット / CD9/CD63 Exosome ELISA Kit, Human  |
CSR | EXH0102EL | 1 KIT [96test] |
¥100,000 |
製品使用文献
- Ryouichi Tsunedomi, et al. Elevated expression of RAB3B plays important roles in chemoresistance and metastatic potential of hepatoma cells. BMC Cancer 2022 Mar 11;22(1):260. https://pubmed.ncbi.nlm.nih.gov/35277124/
- Mohammad Abdullah, et al. Cholesterol Regulates Exosome Release in Cultured Astrocytes. Front Immunol. 2021 Oct 14:12:722581. https://pubmed.ncbi.nlm.nih.gov/34721384/
- Takenori Ishida, et al. Application of peptides with an affinity for phospholipid membranes during the automated purification of extracellular vesicles. Sci Rep. 2020 Oct 30;10(1):18718. https://pubmed.ncbi.nlm.nih.gov/33127950/
- Ryoko Takeuchi, et al. Exosomes from conditioned media of bone marrow-derived mesenchymal stem cells promote bone regeneration by enhancing angiogenesis. PLoS One. 2019 Nov 21;14(11):e0225472. https://pubmed.ncbi.nlm.nih.gov/31751396/
【関連商品】
- ヒト 母乳由来エクソソーム
母乳中のエクソソームの機能やその作用メカニズムの研究に有用 - ExoTrap™ Exosome Isolation Spin Column Kit for Protein Research [CAC]
スピンカラムタイプのエクソソーム単離キット - エクソソームモノクローナル抗体 Anti CD9, CD63, CD81 [CAC]
非標識、ビオチン標識、Tide Fluor™ 標識などを取り揃えております
【関連情報】
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について























 このページを印刷する
このページを印刷する