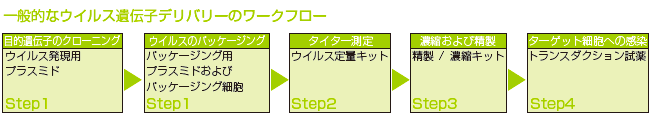
I. リコンビナントアデノ随伴ウイルスの調製
※目的遺伝子をアデノ随伴ウイルス発現ベクターにクローニングします。
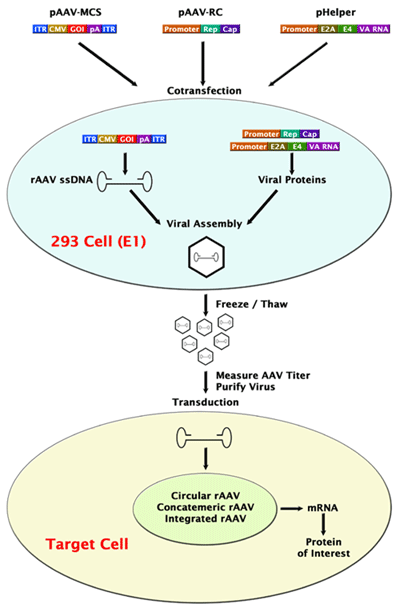
1. トランスフェクション前に、293細胞または、293AAV細胞(品番:AAV-100)を70-80%コンフルになるように培養します。
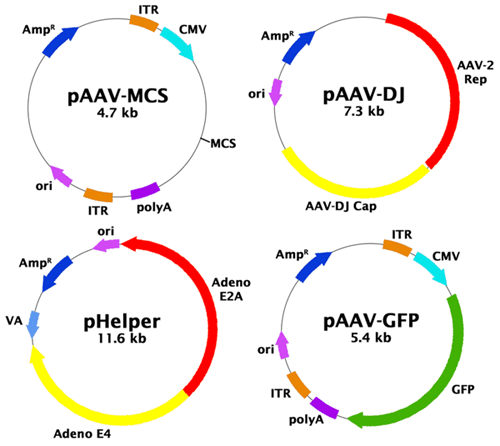
2. pAAV Expression vector、pAAV-DJ、pHelper を共トランスフェクションします。
※ 推奨混合比:pAAV Expression Vector:pAAV-DJ:pHelper = 1:1:1
※ AAVの調製はリン酸カルシウム法が適しています。脂質ベースのトランスフェクション試薬を使用する場合は、FuGENE® 6 (Roche Applied Science) またはLipofectamine™ LTX (Invitrogen)などをご使用下さい。
3. トランスフェクションから48-72時間後、0.5M EDTAを終濃度10mMとなるようプレートに加え、3分間室温でインキュベートします。数回、プレートをやさしく撹拌し、滅菌したチューブに細胞を含む培地を回収します。
※ ウイルス調製の過程で、いくつかの細胞が集まってプレートからはがれ培地中に浮いているのが見られます。
※ ウイルスは、無傷な細胞と培地の両方に存在します。より濃縮されたウイルスストックの調製には、細胞ペレットとして進めることを推奨します。
4. 細胞懸濁液を1000rpmで5分間遠心し、上清を除き、DEMEまたはPBSで再懸濁します。
5. 細胞懸濁液を37℃のウォーターバスとドライアイス-メタノールバスに交互に置いて凍結融解を4回繰り返します。10,000g,10分間遠心分離し、細胞残渣を取り除き、上清をAAVクルードとして回収します。
6. AAVクルードライセート(ウイルスストック)を-80℃で保存します。
II. パッケージング後の確認事項
リコンビナントアデノ随伴ウイルス(rAAV)ベクターの調製の質は、信頼性と再現性のあるデータを得る際に重要な要素です。クルードセルライセートからrAAVを精製する操作は通常、ターゲット細胞にトランスダクションする前に必要になります。rAAVは通常、遺伝子コピー(GC)数によって定量されます。
これらのゲノムを含む粒子は、機能的なベクターで、ターゲット細胞に感染します。
“full AAV”に加えて、空のウイルス粒子も生産されます。
したがって、粒子数の合計ではなくGCの測定の方がより適切です。
1.rAAVの精製・濃縮
rAAVベクターは、CsCl勾配超遠心、密度媒体iodixanolを用いた超遠心及び高速液体クロマトグラフィー(HPLC)によって精製することができます。最もポピュラーな技術であるCsCl超遠心分離は、回収率及び質が悪く時間のかかる方法です。(ウイルス以外のタンパク質のコンタミネーションや、遺伝子コピー数が感染ユニットに比べ高くなります。) AAV-DJの精製は、CBL社 ViraBindアデノ随伴ウイルス精製キット(品番:VPK-140)の使用を推奨します。
2. rAAVの力価測定
a. 遺伝子コピー(GC) 数
宿主細胞への一貫性のあるウイルストランスダクションを確実にすることは重要なステップです。しかし、定量PCRやウイルスDNAのドットブロットには、1-4日間を要します。
ELISA法は、AAVインタクトな粒子のみ検出する抗体を用いて開発されてきました。しかしながら、この方法では、ゲノムDNAが欠損したAAV粒子を含む全てのAAV粒子を測定します。
CBL社のQuick titer AAV 定量キット(品番:VPK-145)は、細胞感染を伴わず、それどころか精製されたウイルスまたはウイルス上清サンプル内のウイルスの核酸を特異的に測定します。アッセイにかかる時間は、精製されていない上清サンプルは4時間で、精製されたサンプルは30分です。
b. 感染力価
rAAVベクターの場合、rAAVの力価は、GFPやLacZなどのレポーター遺伝子の発現で測定します。rAAV-LacZの場合、X-Gal 染色後の青色細胞は、それぞれ1 Infectious unit(IU)を表します。rAAV-GFPの場合、蛍光顕微鏡下で緑色細胞は、それぞれ1ユニットを表します。
3. 感染効率上昇のためのトランスダクション試薬の使用
AAVのトランスダクションの過程は、ウイルスの結合、侵入、細胞内での輸送、核の輸送やウイルスのセカンドストランドDNAの合成から成ります。ウイルスのセカンドストランドDNAの合成は律速段階とみられ、AAVベクターによる非効率なトランスダクションを導きます。
CBL社のViraDuctin™ AAV トランスダクションキット(品番:AAV-200)は、分裂細胞と非分裂細胞どちらでも、AAVを効率的にトランスダクションできるようにデザインされています。
 AAV-DJ ヘルパーフリー発現システム (品番:VPK-410-DJ)
AAV-DJ ヘルパーフリー発現システム (品番:VPK-410-DJ) 293AAV Cell Line (品番:AAV-100)
293AAV Cell Line (品番:AAV-100) ViraBind™ アデノ随伴ウイルス精製キット (品番:VPK-140)
ViraBind™ アデノ随伴ウイルス精製キット (品番:VPK-140) QuickTiter™ アデノ随伴ウイルス定量キット (品番:VPK-145)
QuickTiter™ アデノ随伴ウイルス定量キット (品番:VPK-145) ViraDuctin™ アデノ随伴ウイルストランスダクションキット (品番:AAV-200)
ViraDuctin™ アデノ随伴ウイルストランスダクションキット (品番:AAV-200)