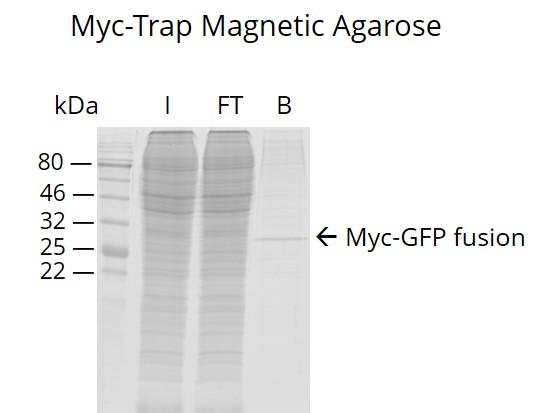
Mycタグとは?
Mycタグは、ヒト生体内で細胞周期の進行、アポトーシス、細胞の形質転換に関与する転写因子であるヒトc-Mycタンパク質中の特定アミノ酸残基(EQKLISEEDL)に相当する配列からなるエピトープタグ/ペプチドタグです。任意の宿主で発現させたMycタグ融合タンパク質は、免疫沈降(IP)、共免疫沈降(CoIP)、アフィニティークロマトグラフィー等の各種アプリケーションに利用することができます。単一のMycタグからなる1xMyc(アミノ酸配列:EQKLISEEDL)、または繰り返し配列のMycタグからなる2xMyc(アミノ酸配列:EQKLISEEDLEQKLISEEDL)が利用されます。
■ VHH抗体とは?
VHH抗体は、NANOBODY® としても知られるラクダ科動物の「重鎖抗体(Heavy chain-only antibody)」由来の抗原結合ドメインです。一般的な抗体と比べて、10分の1程度とサイズが小さく、高い特異性と親和性を示すことで知られます。
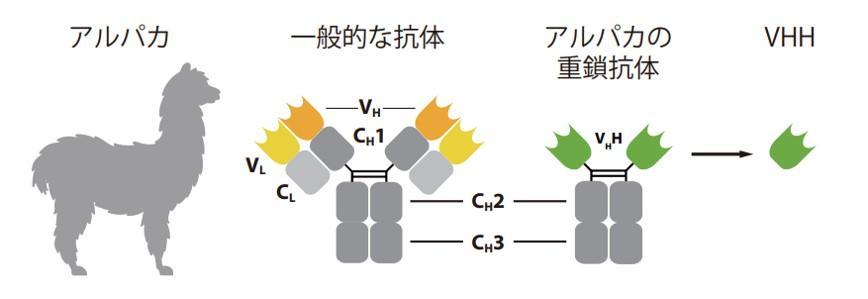
図. ラクダ科動物のユニークな重鎖抗体・VHH
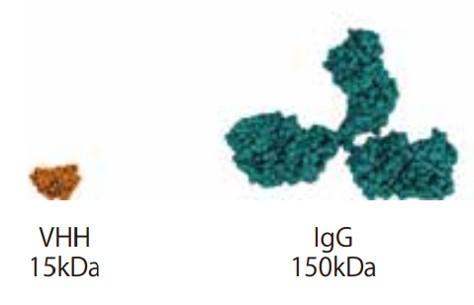
図. 従来の1/10ほどの分子量
■ Nano-Trapとは?
 Nano-Trap(ナノトラップ)は、迅速かつ効率的な免疫沈降(IP)に最適です。各種担体(アガロースビーズ、磁性アガロースビーズ、磁気ビーズ)に結合したVHH抗体で構成されます。
Nano-Trap(ナノトラップ)は、迅速かつ効率的な免疫沈降(IP)に最適です。各種担体(アガロースビーズ、磁性アガロースビーズ、磁気ビーズ)に結合したVHH抗体で構成されます。
各種ビーズ上に結合したVHH抗体は、ビーズ上に残存し、SDSサンプルバッファー中で溶出されません。したがって、従来のIP解析でしばしば問題となるIP抗体由来の軽鎖または重鎖バンドの干渉が無く、シングルバンドの精製を可能とします。さらに、ウエスタンブロットに使用する一次抗体/二次抗体を自由に選択できます。
■ Nano-Trapのアプリケーション
- IP(免疫沈降)/ CoIP(共免疫沈降)
- ChIP(クロマチン免疫沈降)/ RIP(RNA免疫沈降)
- 質量分析(Mass spectrometry)
- On-bead enzyme assay
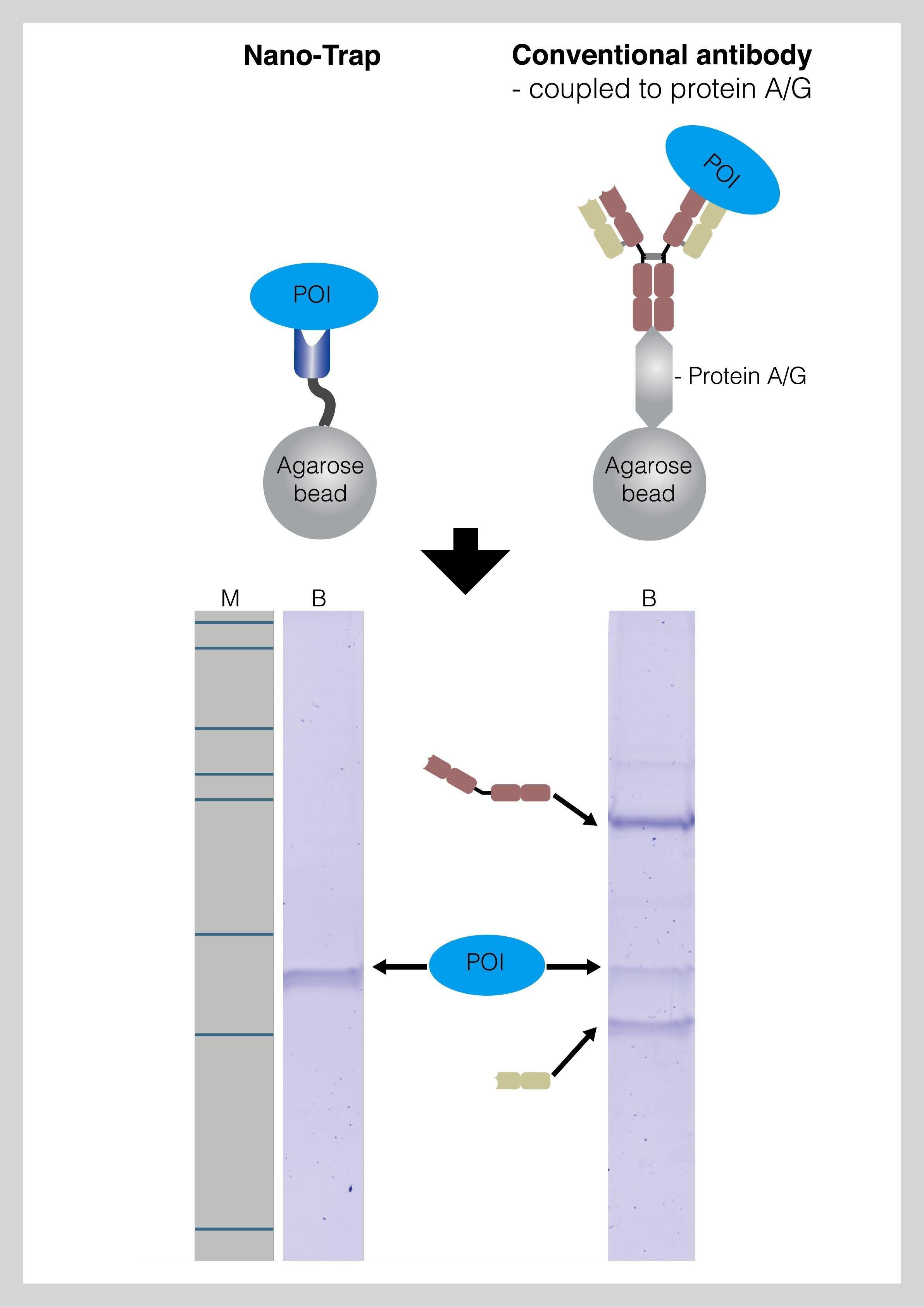
図. Nano-Trap(左)と従来型であるProtein A/G結合IgG抗体(右)を用いた免疫沈降の概要。Nano-Trapでは、単一のバンドを得られ、従来型とは異なり軽鎖/重鎖由来のバンドは観察されません。
■ Proteintech Group(プロテインテック)とは?
Proteintech Group, Inc.(プロテインテック)社は、2001年に設立された抗体製造メーカーです。現在までに、米国本社の他、英国、中国、ドイツ、フランス、シンガポール等で支社を展開し、各国で様々なマーカー抗体、タンパク質研究用試薬を供給しています。国内におけるテクニカルサポート等は、2016年より株式会社プロテインテック・ジャパン(www.ptglab.co.jp  )が担当しています。
)が担当しています。
- 全てオリジナル商品:自社ラボで製造、検証済み(購入後1年間の交換保証付き)
- 数多くの評判:国内・海外における累計158,800報以上の論文使用実績(2026年5月現在)
- 迅速な納期:約22,000品目を当社倉庫に国内在庫!
\最新キャンペーン情報/
プロテインテックは「世界で評価されている抗体サプライヤー」























 このページを印刷する
このページを印刷する