小笠原英明 様
GPCR創薬の現状と展望
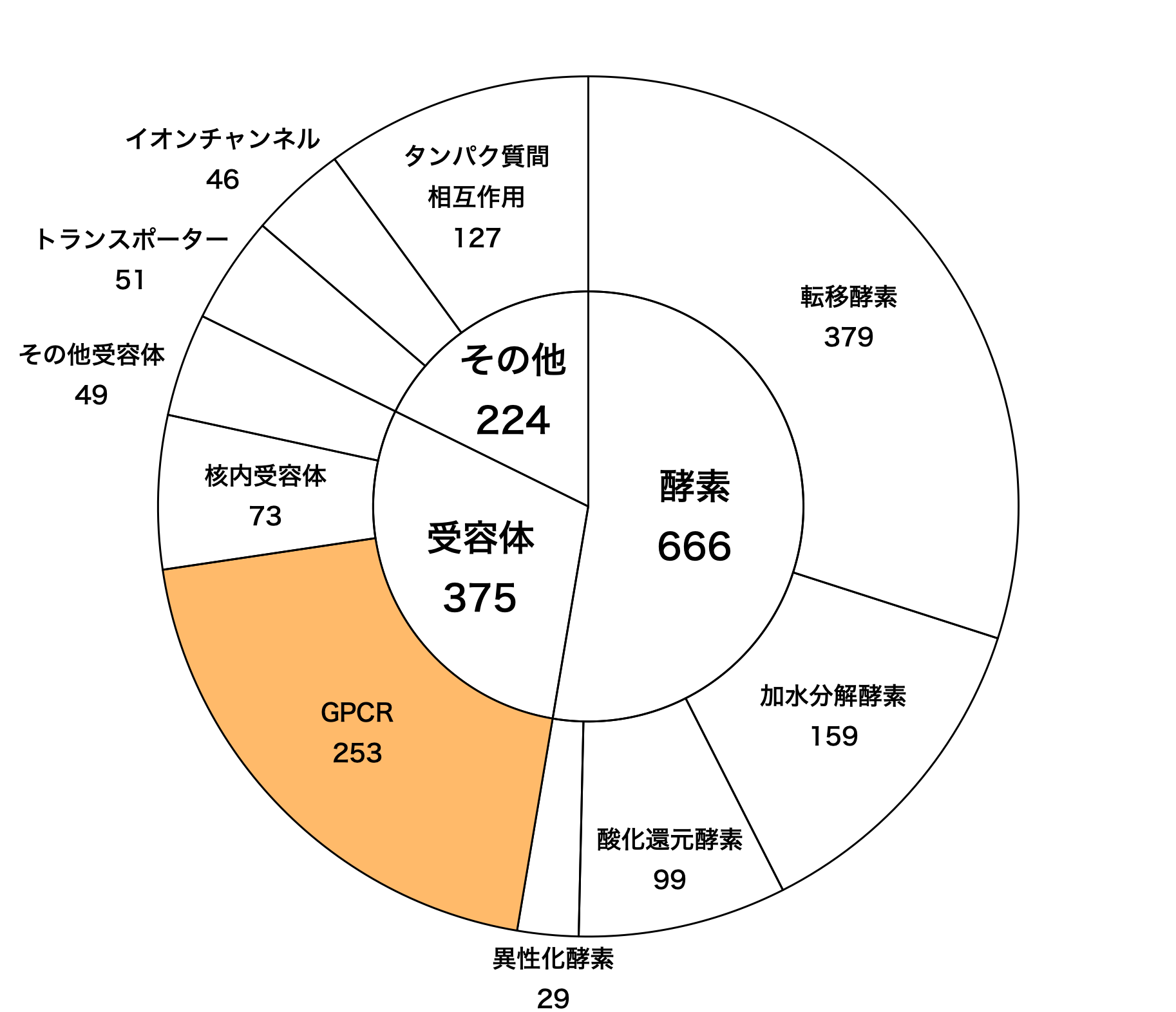
Gタンパク質共役型受容体(GPCR)は医薬品の主要な標的分子群のひとつです。医薬産業政策研究所の調査(図1)によればGPCR標的の新薬開発品目数は開発薬全体の20%(253/1265)を占めています1。新規標的(未だ医薬品が開発されていない受容体)を対象とする創薬プロジェクトが成功すればfirst-in-classの新薬開発に繋がりますが、失敗するリスクも高いです。それ故に、現在のGPCR創薬では、新規標的ではなく既知標的(既に医薬品が開発されている受容体)を対象とするプロジェクトが主流です1。既知標的を対象にした創薬プロジェクトであってもbiased agonismもしくは allosteric modulationといった新しいコンセプトを導入することにより、革新的な医薬品の創出が可能と考えられます2。
図1 標的分子種類別の新薬開発品目数
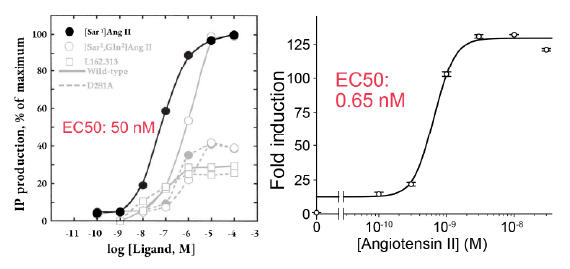
Biased agonismは、作用する受容体が同一であるにも関わらず、リガンド化合物ごとに異なるシグナリングプロファイルが惹起される現象です。GPCRの場合、Gタンパク質もしくはβ-arrestinのどちらか一方を選択的に活性化するbiased ligand(図2)に関して研究が進んでおり3、より副作用の少ない鎮痛薬として米国FDAから認可されたoliceridine (μ-オピオイド受容体に対するbiased ligand)が開発成功例として知られています。しかし一方で、oliceridineの軽微な副作用はbiased agonismではなく化合物自体のlow intrinsic efficacyに起因するとの報告や4、近年、培養細胞で全Gタンパク質を欠失させるとβ-arrestinシグナルも同時に消失するとの予想外の報告がなされるなど5,6、「Gタンパク質・β-arrestin間でのbiased agonism」の意義に関して意見がわかれています。
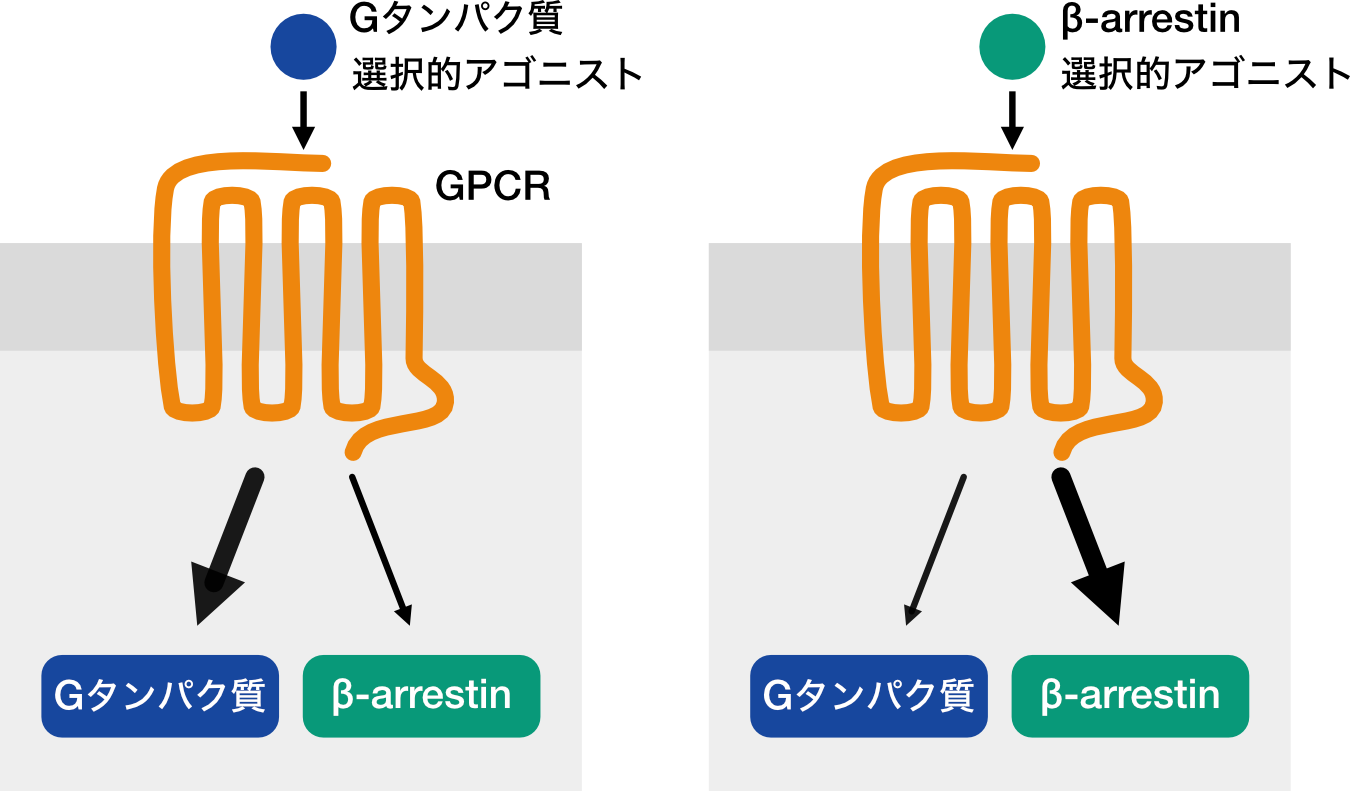
図2 Gタンパク質・β-arrestin間のbiased agonism
Gタンパク質・β-arrestin間のbiased agonismではいずれかのシグナル伝達経路が選択的に活性化される。
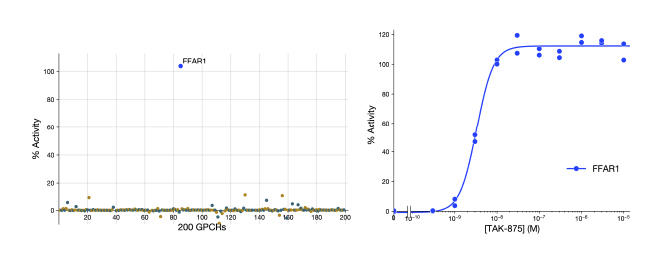
このような状況をうけ、「Gタンパク質・β-arrestin間でのbiased agonism」に加えて、「共役するGタンパク質間でのbiased agonism(作用するGPCRが同一であるにも関わらず、リガンド化合物依存的に異なるGタンパク質が活性化される現象)」が現在注目され(図3)、既にそのような化合物例として、μ-及びκ-オピオイド受容体に対するnaloxone7、オキシトシン受容体に対するatosiban8、グレリン受容体に対するwFw-isonipecotic acid8などが報告されています。今後は「共役するGタンパク質間でのbiased agonism」がGPCR創薬における新たなトレンドになっていく可能性が高いです。
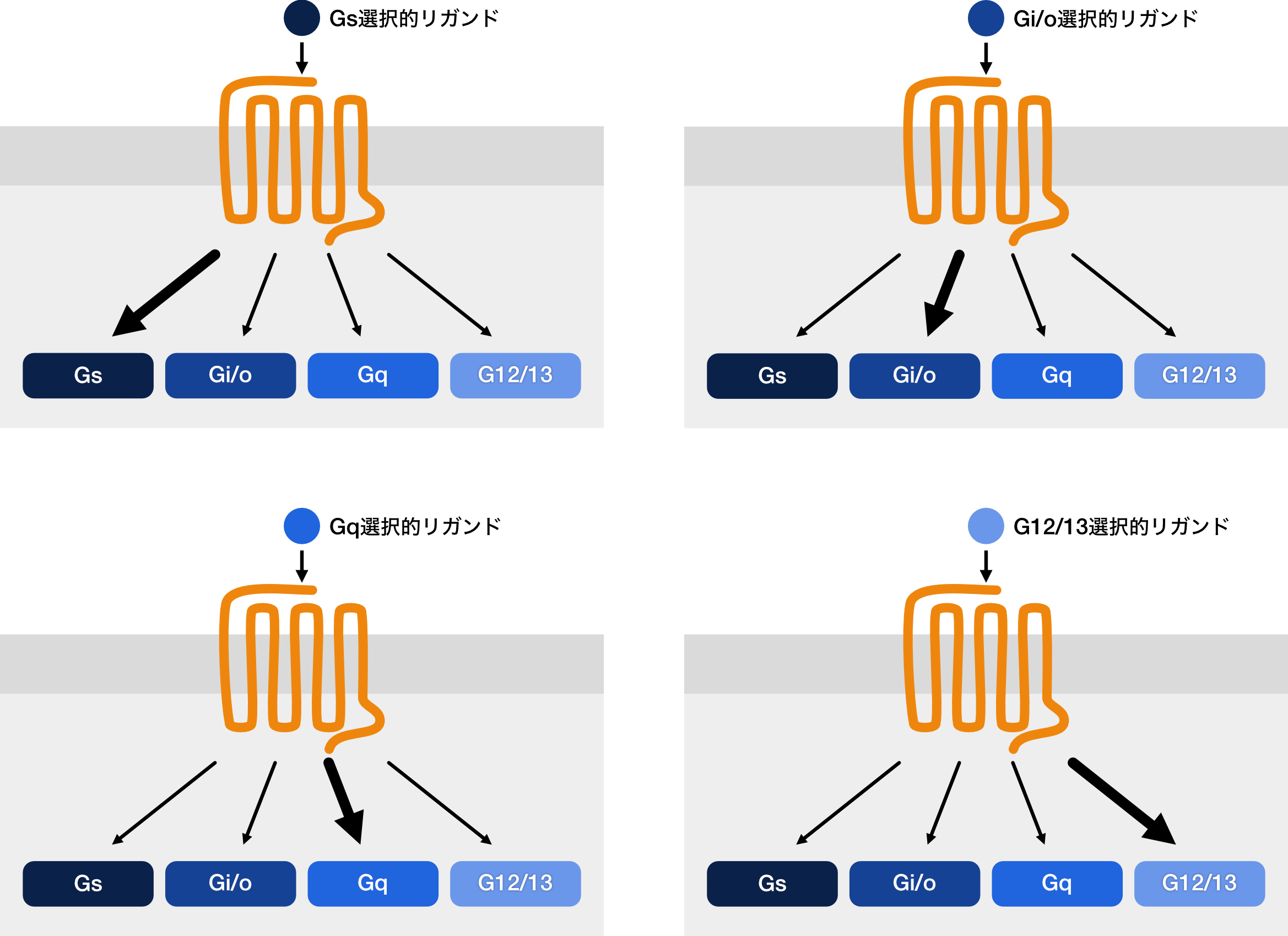
図3 Gタンパク質間のbiased agonism
Gαタンパク質間のbiased agonismではGαタンパク質(Gs, Gi/o, Gq, G12/13)の中の特定のものが選択的に活性化される。
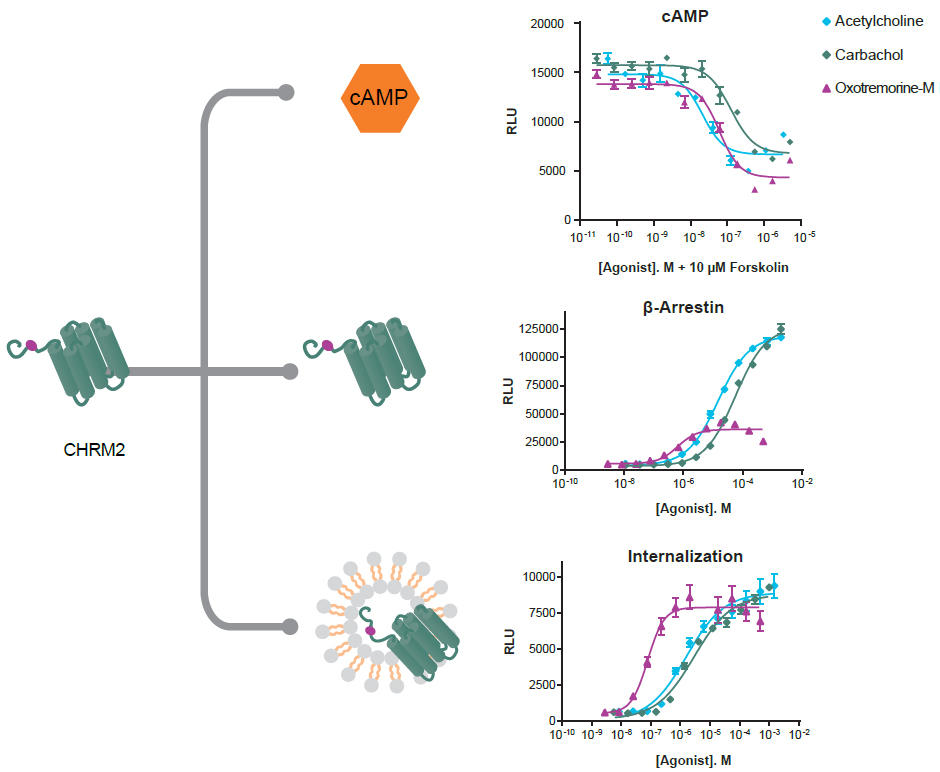
Allosteric modulatorは生理的リガンドとは異なる受容体部位に作用することにより、1) 同じ生理的リガンドを認識するファミリー受容体間であっても受容体特異性を発揮しやすい、2) 生理的リガンド存在下でのみ作用することから薬理効果の時間的選択性をもたらす、といった魅力的な性質を有しています。更に、allostericな作用により生理的リガンドとは質的に異なるbiased agonismを惹起しうるため(図4)、従来の医薬品にはない有用性を生み出すことが期待できます2,3。
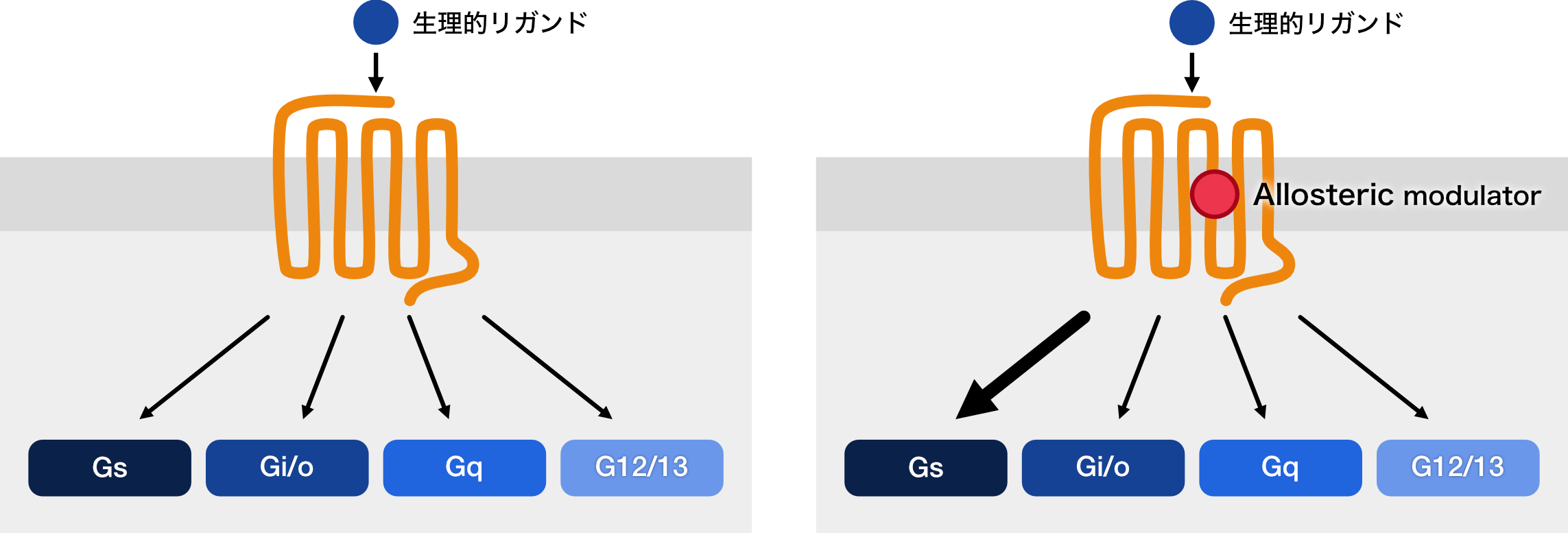
図4 Allosteric modulatorによるbiased agonism
生理的リガンドのみの時とは異なる下流シグナル伝達経路の活性化をもたらすallosteric modulatorは医薬品の新しい作用機序として期待される。Allosteric modulatorによるGsに偏った活性化の例を図に示したが、同様に、他のGタンパク質間、あるいはGタンパク質・β-arrestin間のbiased agonismに寄与するallosteric modulatorも考えられる。
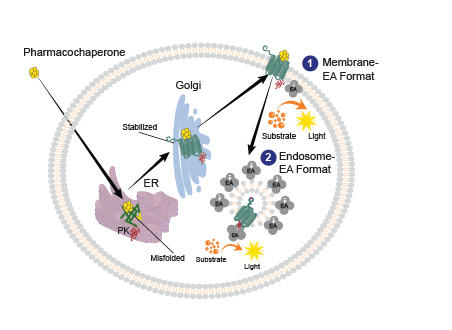
創薬標的としてのポテンシャルを有するGPCR(嗅覚受容体などの感覚受容体を除く)はヒトゲノム上に約300-400種類存在しますが、そのうちの約200種類は未開発のままです2。未開発のGPCR、特にオーファン受容体に関しては、受容体を活性化するリガンドが同定されておらず、受容体下流のシグナル伝達経路に関する情報も不足しています。そのため従来のアッセイ系による受容体活性の検出は困難を極め、これらGPCRに対して適用可能な新規アッセイ系の確立が待たれています。新規アッセイ系による化合物スクリーニングを通じて、これら受容体に対するsurrogateリガンドが同定されれば、そのリガンドをプローブとして当該受容体の生理機能を解明できます。未開発なGPCRの生理機能及びヒト疾患との関連性を次々と明らかにし創薬標的として選定されうるGPCRのレパートリーを拡大することが、GPCR創薬の更なる発展に重要です。
メーカー一覧
コスモ・バイオでは、GPCR創薬研究に有用な製品・サービスを取り扱っております。























 このページを印刷する
このページを印刷する