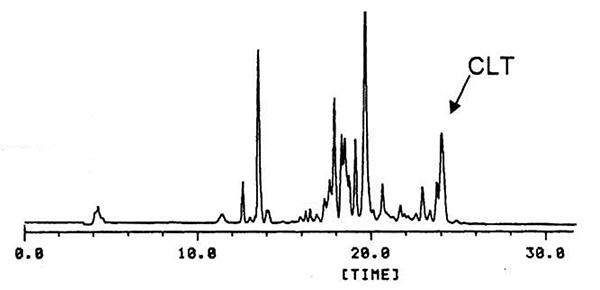
これまで述べたように、ラクトフェリシンを抗原として作成されたモノクローナル抗体に対する反応性を有するペプチド画分が得られ、またそのペプチドの質量が4069であることも判明しました。次の段階としてこのペプチドがラクトフェリンのどの部分に相当するのかを決定するために、本章で述べるアミノ酸配列の決定を行ない、N末端から11残基までの配列(TAGWNIPMGLI)が決まりました。このペプチドの質量と付き合わせると、ラクトフェリン全配列のどの部分かを決めることができます。
なお、Cローブを調製した際にもそのN末端アミノ酸配列(YTRVVWXAVGPEEQKKQX)およびC末端アミノ酸配列(FLTR)を確認しています1)。この場合、以下に述べるようにN末端アミノ酸配列はPTH誘導体として、C末端アミノ酸配列はPTC誘導体としてC18カラムで分析しました。
アミノ酸配列の分析にはエドマン(Edman)法を自動化した装置(ペプチドシークエンサあるいはプロテインシークエンサともいう)が用いられます。エドマン法とは、タンパク質あるいはペプチドのN末端部分の遊離アミノ基にフェニルイソチオシアネート(PITC)を反応させ、フェニルチオカルバミル誘導体(PTCアミノ酸)とし、次いでトリフルオロ酢酸(TFA)によってアニリノチアゾリノン(ATZ)-アミノ酸として遊離させ、さらに酸性下で安定なフェニルチオヒダントイン(PTHアミノ酸)に変換して分析するものです。装置としては上記の反応を繰り返して自動的に行なわせる部分と、遊離したPTHアミノ酸をC18カラムで分析する高速液体クロマトグラフィー(HPLC)、およびその制御とデータ処理のためのパーソナルコンピュータで構成されています。1サイクル約1時間で終了し、PTHアミノ酸の検出は、269 nmでの吸光度を測定することによって行います。なお、分析用の試料が溶液状態の場合はポリブレン処理したカートリッジフィルター(ガラスファイバーフィルタ)に、またはPVDF膜に吸着させて分析を行ないます。この際に必要な試料量としては、機種によりますが10 pmol程度です。
アミノ酸配列のための試料は高純度に精製したタンパク質やペプチドで、最終的に逆相クロマトグラフィーで精製することが推奨されています。その他に、SDS電気泳動や二次元電気泳動を行ったゲルからPVDF膜に転写して色素染色し、目的のバンド(スポット)を切り取り、よく洗浄して緩衝液成分のグリシンなどを完全に除いてから配列解析に用います。
また第5、8章で述べたように、電気泳動を行ったポリアクリルアミドゲルからタンパク質を抽出し、あるいはゲル中でプロテアーゼを作用させて得られた反応物から逆相クロマトグラフィーで各成分を分画し、そのフラグメントのアミノ酸配列を決める方法もあります。あるいはPVDF膜に固定化した目的タンパク質を還元アルキル化した後、酵素消化します。回収したペプチド混合物を逆相クロマトグラフィーで分画し、アミノ酸配列の分析を行います。
ジスルフィド結合(S-S結合)がある場合、還元した後にピリジルエチル化2)(第6章参照)すると、アミノ酸シークエンサで同定が可能となります。ただし、ジスルフィド結合を形成している残基対が複数ある場合に、それら対を形成する相手同士を決定するためには、別の実験操作を組み合わせなければなりません。
エドマン分解では、全ての結合が均等に反応しない場合があり、プロリル結合、アスパラギン−グリシン結合などでは収量が低下するといわれています。また、N末端のアミノ基が修飾されていたり環状ペプチド、あるいはウシκカゼインのように環状アミノ酸残基である場合には、エドマン法による分析は出来ません。タンパク質のN末端アミノ基が修飾されている場合、最も多いのがアシル基すなわちホルミル化、アセチル化、ピログルタミル化、ミリスチル化などの修飾がされた基であり、それぞれに特異的な化学的あるいは酵素的な脱離法を用いなければなりません。
C末端側のアミノ酸配列を決定するには、カルボキシペプチダーゼY(carboxypeptidase Y)などによる逐次分解法を行い、C末端側から順次遊離するアミノ酸残基を同定する方法が用いられます。具体的には、ペプチドを0.2% SDS/0.2 Mエチルモルフォリン(pH 5.9)溶液に溶解して加熱変性させ、次いで0.1Mリン酸緩衝液(pH 5.6)に溶解した適量のカルボキシペプチダーゼを加え、37℃で反応させます。一定量の反応混液を経時的に採取し、その1/5量の酢酸に加えてペプチドを沈殿させて反応を停止し、上清中の遊離したアミノ酸をアミノ酸分析計で同定し、配列を決めます。アミノ酸分析計の代わりに質量分析計(第8章を参照)を用いて同定する方法もあります。カルボキシペプチダーゼの濃度を変えて反応させると、ペプチド鎖長の異なる集団ができます。この反応を質量分析用試料プレート上で行い、イオン化促進試薬を加えて質量スペクトルを測定しC末端アミノ酸配列を同定します。これをラダーシークエンス法といいます。
また、固定化アンヒドロトリプシンのLysやArgに対する強い親和性を利用し、これらをC末端に含むペプチドを除いて本来のC末端部分を含むフラグメントを得、N末端側からアミノ酸配列を決める方法もあります。トリプシンかリジルエンドペプチダーゼで限定分解しますが、目的タンパク質あるいはペプチドのC末端アミノ酸がLysやArgである場合には、キモトリプシンで分解します。タンパク質/ペプチドを無水酢酸とチオシアン酸で処理し、C末端アミノ酸をチオヒダントイン誘導体に変え、最終的にアルキルチオヒダントイン誘導体(ATH-アミノ酸)にして遊離させ(アルキル化チオヒダントイン法)、逆相クロマトグラフィーで同定する方法も開発されています。
タンパク質化学の初期の頃はタンパク質のN末端アミノ酸を同定する方法が種々工夫されました。代表的なものは5-ジメチルアミノナフタレンスルホニルクロリド(DNS-Cl)をタンパク質に作用させ、塩酸加水分解をした後、アミノ酸分析を行うダンシル化法です。この時、蛍光性のNα-DNS-アミノ酸が生成し、ペーパークロマトグラフィーや薄層クロマトグラフィー(thin-layer chromatography, TLC)でダンシル化アミノ酸を同時に展開してその位置の比較から同定を行います。
タンパク質やペプチドを構成している全アミノ酸組成を知るためには、定沸点塩酸溶液中で110℃に加熱して6〜20時間加水分解します。あるいは気相分解法が用いられます。イオン交換樹脂カラムを用いてアミノ酸分析を行い、検出にはニンヒドリン発色法を用います。このように分離カラムから溶出した後で発色団を反応させる方法をポストカラム法といい、予め蛍光物質やその他の発色団をアミノ酸に標識してから逆相クロマトグラフィーで分離し検出する方法もあります(プレカラム法)。
全く異なる方法として、対象タンパク質の遺伝情報を有するDNAあるいはRNAの塩基配列からアミノ酸配列を決めることも現在では一般的に行われています(他の成書を参照して下さい)。