記事ID : 16905
モータータンパク質キネシンと神経変性 CYTOSKELETON NEWS 2016年6月号

モータータンパク質キネシンと神経変性
はじめに
モータータンパク質であるキネシンは、有糸分裂と、神経細胞における高速軸索輸送(FAT)のような順行性のカーゴ(積み荷)の輸送を調節しています。神経細胞は、細胞周期の調節、特に紡錘体の集合と機能を、キネシンに依存しています(紡錘体: 主に微小管(MT)から構成される巨大な構造物。重合と脱重合のサイクルを繰り返して、2個の娘細胞に二倍になった染色体を適切に分配する)。また、キネシンモーターは、微小管を利用して、タンパク質、脂質、ミトコンドリアなどのカーゴ(積み荷)を、合成が行われる細胞体から軸索や軸索末端へ輸送しており、このプロセスは正常な神経細胞の発生、成長、情報伝達に必須となります1。
細胞周期の異常(例:染色体分配異常、紡錘体の構造/機能異常、異数性)および 軸索輸送障害は、アルツハイマー病(AD)の病態生理学的特徴であり、認知症でも共通して認められます2,3。実際に、認知症の典型的な神経病理学的特徴(老人班と濃縮体)の前に、軸索輸送障害 および 軸索の膨化が起こることから、複数の研究者が、軸索輸送障害は神経細胞の脆弱性 および 神経変性の初期徴候であると仮定しています4-8。本稿では、Eg5(KSP、kinesin spindle protein、KIF11、キネシン-5)とキネシン-1 が、アルツハイマー病に関連する細胞周期異常 および 軸索輸送障害において担う役割に注目します。Eg5 は、微小管と相互作用するキネシンモーターで、紡錘体の形成と機能に不可欠です。キネシン-1は、原型となるキネシンで、軸索輸送を仲介します。神経変性におけるダイニンモーターの役割については、「CYTOSKELETON NEWS 2014年1月/2月号」をご参照ください。
モーターと神経変性: 細胞周期の異常
アルツハイマー病の神経病理学的な特徴は、βアミロイド(Aβ)班と、過剰にリン酸化されたタウの蓄積による神経原線維変化です。Aβは、アミロイド前駆体タンパク質(APP)が、β-セクレターゼ1(BACE1)とプレセニリン(PS)を含むγ-セクレターゼ複合体によって切断されることで形成されます2,3。アルツハイマー病に関連する細胞周期の異常では、Aβとタウの両方が、Eg5 の活性 および 微小管との相互作用を阻害し、紡錘体の構造と機能に負の影響を与えます9-11(図1)。紡錘体の機能不全は、染色体分配異常、異数性/高倍数性、細胞死につながります9-11。タウによる Eg5 の阻害には、過剰量の微小管に結合したタウが必要になります10。異数性/高倍数性を示す神経細胞は、プレクリニカル期(前臨床期)のアルツハイマー病で増加し、アルツハイマー病の進行に伴い、選択的な細胞死が起こります。実際に、アルツハイマー病の剖検脳でみられる細胞死の 90% が、高倍数体の神経細胞で構成されています12。
アルツハイマー病における Eg5 の役割は、成熟した有糸分裂後の神経細胞でも発現していることから、細胞周期の異常に限定されません。Eg5 は、少なくとも部分的に、NMDA受容体 および 神経成長因子/p75 ニューロトロフィン受容体の細胞表面への輸送の減少を介して13、Aβによって誘導される長期増強の阻害、および、海馬のスパイン(棘突起)/シナプスの減少を仲介します13,14。
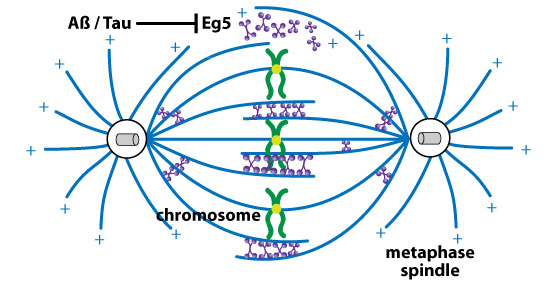
図1 キネシンモーター Eg5 の微小管への結合は、紡錘体の適切な構造と機能に必須であり、Aβ および タウによって阻害される。
モーターと神経変性: 軸索輸送障害
4つの神経変性疾患関連タンパク質(APP、Aß、PS、タウ)は全て、キネシン-1 が仲介する軸索輸送を阻害します。APP および Aβ による軸索輸送の障害については15-17、アクチン凝集やアクチン重合の動的な変化から16、カゼインキナーゼ2の活性化(キネシン-1軽鎖がリン酸化され、キネシン-1 からカーゴが放出される、連続的なカスケードが開始される17)にわたる、様々なメカニズムが報告されています。興味深いことに、APP は、軸索膜の区画の一部(BACE1 と PS1 も含まれます)として19-21、キネシン-1軽鎖との結合を介して順行性軸索輸送を受けます18。このように、APP は、キネシン-1を介した軸索輸送の間または後に、Aβに切断される可能性があります21。しかし、この知見については、他の研究グループにより誤りを指摘されています22。
タウと変異 PS1(M146V)はどちらも、脱リン酸化により刺激される GSK-3ß の活性化を介して、キネシン-1 が仲介する軸索輸送を調節します。その結果、キネシン-1 軽鎖が GSK-3ß を介してリン酸化され、キネシン-1 とカーゴの解離が誘導されます5(図2)。GSK-3ß は、タウキナーゼとして、病理学的な特徴である過剰リン酸化タウの形成を仲介します。過剰リン酸化タウは、微小管から解離して微小管の脱重合を引き起こした後に、タウフィラメントを形成し、最終的には神経原線維変化を生じます2,3。タウのフィラメント、または、C末端が切断された非結合型モノマー(C末端には微小管結合ドメインが含まれる)のN末端は、キネシン依存的な軸索輸送を阻害します。この場合は、プロテインホスファターゼ1(PP1)を介した脱リン酸化によって誘導される GSK-3ß の活性化を介して、GSK-3ß 活性が増加します23(図2)。これらの研究から、複数の研究者たちが、アルツハイマー病の病態生理においては、初期に軸索輸送障害が起こることを示唆しています2-5。実際に、軸索/輸送の障害は、アミロイド沈着のかなり前に起こります4。また、キネシン-1 の枯渇により、同様の輸送障害が生じますが、同時にAβペプチドの量が増加し、蓄積が促進されます4。
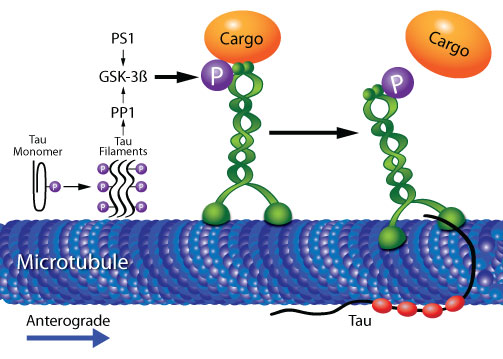
図2 キネシン-1 を介した順行性の軸索輸送は、GSK-3ß を介したキネシン-1 軽鎖のリン酸化によって阻害され、キネシン-1 とカーゴ(積み荷)の解離を引き起こす。GSK-3ß は、PS1や、過剰にリン酸化されたタウフィラメントによって活性化される PP1 によって、活性化される可能性がある。
まとめ
正常な神経細胞の生理機能は、適切な有糸分裂や軸索輸送などの様々なプロセスで、キネシンモーターに依存しています。キネシンの機能障害は、ADだけではなく、ハンチントン病24、(上下位)運動ニューロン病、末梢神経疾患であるシャルコー・マリー・トゥース病2,3 でも見られることから、神経細胞の健全性に重大で広範囲に及ぶ影響を与えます。Cytoskeleton社では、モータータンパク質であるキネシンとダイニンが、神経細胞の健全性と生存をどのように制御しているのかを研究するために使用できる、精製したモータータンパク質(キネシン、ダイニン)、微小管に誘導されるモータータンパク質の ATPase 活性を測定できるキットをご提供しております。
参考文献
- Bass P.W. 1998. The role of motor proteins in establishing the microtubule arrays of axons and dendrites. J. Chem. Neuroanat. 14, 175-180.
- Millecamps S. and Julien J.-P. 2013. Axonal transport deficits and neurodegenerative diseases. Nat. Rev. Neurosci. 14, 161-176.
- Morfini G.A. et al. 2009. Minisymposium: Axonal transport defects in neurodegenerative diseases. J. Neurosci. 29, 12776-12786.
- Stokin G.B. et al. 2005. Axonopathy and transport deficits early in the pathogenesis of Alzheimer’s disease. Science. 307, 1282-1288.
- Pigino G. et al. 2003. Alzheimer’s presenilin 1 mutations impair kinesin-based axonal transport. J. Neurosci. 23, 4499-4508.
- Lazarov O. et al. 2007. Impairments in fast axonal transport and motor neuron deficits in transgenic mice expressing familial Alzheimer’s disease-linked mutant presenilin 1. J. Neurosci. 27, 7011-7020.
- Ishihara T. et al. 1999. Age-dependent emergence and progression of a tauopathy in transgenic mice overexpressing the shortest human tau isoform. Neuron. 24, 751-762.
- Zhang B. et al. 2004. Retarded axonal transport of R406W mutant tau in transgenic mice with a neurodegenerative tauopathy. J. Neurosci. 24, 4657-4667.
- Borysov S.I. et al. 2011. Alzheimer Aß disrupts the mitotic spindle and directly inhibits mitotic microtubule motors. Cell Cycle. 10, 1397-1410.
- Bouge A.-L. and Parmentier M.-L. 2016. Tau excess impairs mitosis and kinesin-5 function, leading to aneuploidy and cell death. Dis. Model. Mech. 9, 307-319.
- Rossi G. et al. 2008. A new function of microtubule-associated protein tau: involvement in chromosome stability. Cell Cycle. 7, 1788-1794.
- Arendt T. et al. 2010. Selective cell death of hyperploid neurons in Alzheimer’s disease. Am J. Pathol. 177, 15-20.
- Ari C. et al. 2014. Alzheimer Aß inhibition of eg5/kin5 reduces neurotrophin/transmitter receptor function. Neurobiol. Aging. 35, 1839-1849.
- Freund R.K. et al. 2016. Inhibition of the motor protein Eg5/Kinesin-5 in amyloid b-mediated impairment of hippocampal long-term potentiation and dendritic spine loss. Mol. Pharmacol. 89, 552-559.
- Gunawardena S. and Goldstein L.S.B. 2001. Disruption of axonal transport and neuronal viability by amyloid precursor protein mutations in Drosophila. Neuron. 32, 389-401.
- Hiruma H. et al. Glutamate and amyloid b-protein rapidly inhibit fast axonal transport in cultured rat hippocampal neurons by different mechanisms. J. Neurosci. 23, 8967-8977.
- Pigino G. et al. 2009. Disruption of fast axonal transport is a pathogenic mechanism for intraneuronal amyloid beta. Proc. Natl. Acad. Sci. USA. 106, 5907-5912.
- Koo E.H. et al. 1990. Precursor of amyloid protein in Alzheimer disease undergoes fast anterograde axonal transport. Proc. Natl. Acad. Sci. USA. 87, 1561-1565.
- Ferreira A. et al. 1993. Intraneuronal compartments if the amyloid precursor protein. J. Neurosci. 13, 3112-3123.
- Kamal A. et al. 2000. Axonal transport of amyloid precursor protein is mediated by direct binding to the kinesin light chain subunit of kinesin-I. Neuron. 28, 449-459.
- Kamal A. et al. 2001. Kinesin-mediated axonal transport of a membrane compartment containing ß-secretase and presenilin-1 requires APP. Nature. 414, 643-648.
- Lazarov O. et al. 2005. Axonal transport, amyloid precursor protein, kinesin-1, and the processing apparatus: Revisited. J. Neurosci. 25, 2386-2395.
- LaPointe N.E. et al. 2009. The amino terminus of tau inhibits kinesin-dependent axonal transport: Implications for filament toxicity. J. Neurosci. Res. 87, 440-451.
- Morfini G.A. et al. 2009. Pathogenic Huntingtin inhibits fast axonal transport by activating JNK3 and phosphorylating kinesin. Nat. Neurosci. 12, 864-871.
キネシン・ダイニンタンパク質
[商品詳細]
- モータータンパク質解析 Cytoskeleton Motor Werks™
- 細胞分裂抑制剤の開発研究に!
キット
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
ATPase ELIPATM (Enzyme Linked Inorganic Phosphate Assay) |
CYT | BK051 | 1 KIT [96 assays] |
CYT社 BK05152 1 を参照 |
GTPase ELIPATM (Enzyme Linked Inorganic Phosphate Assay) |
CYT | BK052 | 1 KIT [96 assays] |
CYT社 BK05152 1 を参照 |
CytoPhos Endpoint Phosphate Assay |
CYT | BK054 | 1 KIT [1000 assays] |
¥134,000 |
Kinesin ELIPA kit |
CYT | BK060 | 1 KIT [96 assays] |
¥278,000 |
HTS kinesin ATPase Endpoint Assay Biochem Kit |
CYT | BK053 | 1 KIT [1000 assays] |
¥307,000 |
微小管
[商品詳細]
- 高純度チューブリン試薬
- ローダミン標識 Tubulin もラインアップ
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Microtubules (Taxol Stabilized and Lyophilized), Porcine |
CYT | MT002-A | 4*500 UG |
¥153,000 |
Microtubules (Taxol Stabilized and Lyophilized), Porcine |
CYT | MT002-XL | 1*10 MG |
お問い合わせ |
■ CYTOSKELETON NEWS バックナンバー
- 2020年10月号 紡錘体 - 可視化に向けた新規ツール
- 2020年8月号 細胞膜染色用蛍光プローブ
- 2020年4月号 生細胞におけるF-アクチンプローブ
- 2020年3月号 コロナウイルスと細胞骨格
- 2020年2月号 タウ(Tau)の将来性をMapping
- 2020年1月号 Rho GTPaseによる細胞遊走制御
- 2019年12月号 表現型プロファイリング:アクチンに焦点を当てたがん治療
- 2019年11月号 チューブリンの過剰グルタミル化、ミトコンドリア、神経変性
- 2019年9月号 細胞運動性を制御するために相互作用する膜張力とアクチン細胞骨格
- 2019年8月号 Rac1B、がん、およびRac1
- 2019年7月号 Rhoファミリー GTPases、神経可塑性、およびうつ状態
- 2019年6月号 アクチンメチオニン酸化: 動的制御の次の段階
- 2019年5月号 ミクログリアと神経変性疾患
- 2019年2月号 生細胞画像化に対するCNS疾患や障害
2018年
- 2018年12月号 アクチン細胞骨格とメカノトランスダクション(機械的シグナル伝達)
- 2018年11月号 軸索再生と細胞骨格
- 2018年10月号 ニューロンにおける微小管と極性
- 2018年8月号 Rab GTPase と 神経変性
- 2018年7月号 SUMO レスリング: バランスが全て
- 2018年6月号 なぜ K-Ras は発がん特異性を示すのか?
- 2018年5月号 治療標的としてのユビキチンプロテアソームシステム:チューブリンは関与するか?
- 2018年4月号 RhoファミリーGEFと樹状突起スパインの構造的可塑性
- 2018年3月号 βカテニンとTFC/LEF-1の翻訳後修飾による標準的なWntシグナル制御
- 2018年2月号 がん抑制遺伝子p53の翻訳後修飾による機能の調整
- 2018年1月号 自閉スペクトラム症におけるGEF Trioの役割
2017年
- 2017年12月号 プロフィリン: アクチン結合タンパク質の多機能な役割
- 2017年11月号 ミトコンドリアにおけるアセチル化:新たな考え方と治療への応用の可能性
- 2017年9月号 翻訳後修飾のアセチル化による微小管の安定化
- 2017年8月号 神経軸索におけるアクチンリングを基盤とした周期的膜骨格(PMS)
- 2017年7月号 E3ユビキチンリガーゼMdm2によるがん抑制遺伝子p53の翻訳後制御
- 2017年6月号 多能性幹細胞(PSC)での転写因子による翻訳後制御
- 2017年5月号 Arf6 GEF と癌細胞の浸潤・転移
- 2017年4月号 PTEN(Phosphatase and Tensin Homolog)による翻訳後制御
- 2017年3月号 Tau の翻訳後修飾: アルツハイマー病の治療標的
- 2017年2月号 樹状細胞の移動におけるアクチン結合タンパク質とF-アクチン
2016年
- 2016年11月/12月号 GEF を介した GTPase シグナル伝達の低分子阻害剤
- 2016年9月号 FtsZ タンパク質: 抗菌薬の新規ターゲット
- 2016年7月号 翻訳後修飾(PTM)は心臓病において細胞骨格タンパク質を調節する
- 2016年6月号 モータータンパク質キネシンと神経変性
- 2016年5月号 チロシンリン酸化は Rhoファミリー GTPase 活性を調節する
- 2016年4月号 Rac1と糖尿病: ポジティブな役割とネガティブな役割
- 2016年3月号 SUMO化: 細胞骨格タンパク質の機能を調節するレギュレーター
- 2016年1月/2月号 ビメンチン中間径フィラメント: リン酸化による調節
2015年
- 2015年8月号 タンパク質調節に不可欠な翻訳後修飾
- 2015年7月号 アクチン細胞骨格のライブセルイメージング
- 2015年6月号 有糸分裂に関わるタンパク質のSUMO化: 局在と機能
- 2015年5月号 Ras 癌の治療: 5つの有望なターゲット
- 2015年4月号 Ras 依存性の癌で注目される YAP1
- 2015年3月号 増刊号 統合失調症において遺伝子変異により誘導されるアクチン依存のシナプスの変化
- 2015年3月号 Ral GTPase を調節する翻訳後修飾
- 2015年1月/2月号 RhoA のリン酸化はシグナル伝達を調節する
- 2015年1月号 増刊号 微小管を不安定化する suprafenacine: 新規抗癌剤のリード化合物としての可能性
2014年
- 2014年12月号 増刊号 RhoA は心筋細胞におけるアクチン細胞骨格の再構成とグルコース取り込みを仲介する
- 2014年11月号 増刊号 樹状突起の形態形成: ドーパミンD1受容体 および Rho ファミリー GTPase による制御
- 2014年11月/12月号 GTPase 活性化アッセイ: アイソフォームの検出
- 2014年10月号 アルギニンの正電荷を消失させるシトルリン化
- 2014年9月号 キネシンサブドメインの探索
- 2014年9月号 増刊号 アクチン結合タンパク質コフィリンの S-ニトロシル化: 細胞移動に対する影響
- 2014年8月号 増刊号 原発性硬化性胆管炎における N-Ras 発現および活性
- 2014年8月号 SUMO化: 細胞骨格タンパク質を標的とした翻訳後修飾
- 2014年7月号 Sos/K-Ras 結合を介して Ras シグナル伝達を制御する新しい低分子阻害剤
- 2014年6月号 増刊号 頭頸部扁平上皮癌における microRNA-138 による RhoC のダウンレギュレーション
- 2014年6月号 Rho GTPase と活性酸素種: クロストークとフィードバック
- 2014年5月号 ミオシンのアセチル化はサルコメアの構造と機能を調節する
- 2014年4月号 リジンのアセチル化 - 多様な細胞プロセスの制御因子
- 2014年3月号 インテグリンを介したβ-アクチンの酸化還元制御: PDIの出現
- 2014年1/2月号 ダイニン: 一つのモーターが関わる複数の神経変性疾患
2013年
- 2013年11/12月号 ダイニン:チームとして強力に作用するモータータンパク質
- 2013年10月号 神経変性:Rhes、SUMO化、ハンチントン病
- 2013年9月号 モノユビキチン化:タンパク質調節のダイナミックなタグ
- 2013年8月号 Ras及びRhoのプレニル化による翻訳後修飾:癌創薬における役割
- 2013年7月号 アクチンが引き起こす膜突起による浸潤:コルタクチン
- 2013年6月号 アクチン修飾と細胞骨格
- 2013年5月号 微小管内部の実体
- 2013年4月号 神経変性におけるTauの多面性
- 2013年3月号 蛍光フィブロネクチンタンパク質を用いた特発性肺線維症の創薬
- 2013年1/2月号 樹状突起棘:発生におけるArf6の役割
2012年
- 2012年11/12月号 ミオシンの小分子モジュレーター
- 2012年10月号 Rhoファミリーパスウェイのユビキチン化と制御
- 2012年9月号 神経変性におけるRac1 GTPaseの機能
- 2012年8月号 上皮間葉転換(EMT)とRhoファミリー低分子量G-タンパク質の関与
- 2012年7月号 チューブリンの多重修飾:グルタミル化とグリシル化
- 2012年6月号 細胞接着のフィブロネクチン制御と原線維形成
- 2012年5月号 アクチン酸化サイクルの機能
- 2012年4月号 トラフィッキング:ArfとCdc42/Racの結合
- 2012年3月号 G-LISAを用いた心臓研究: 糖尿病性心筋症におけるRho経路に関する研究
- 2012年1月/2月号 FtsZ: 新たな抗生剤の標的となるチュ−ブリンホモログ
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について























 このページを印刷する
このページを印刷する














