記事ID : 35274
生細胞画像化に対するCNS疾患や障害 CYTOSKELETON NEWS 2019年2月号

生細胞画像化に対するCNS疾患や障害
ヒトの中枢神経系(CNS)疾患と障害の原因を研究し強力な治療法を開発するためには、それぞれの神経病態生理学を正確に再現でき、かつ、臨床研究へと応用可能なin vitroおよびin vivoでの疾患モデルが必要です1-3。さらに、早期の神経病態生理学変化は初期診断や治療介入の最良の機会となることから、これらを研究することが非常に重要です4。ニューロンのシナプスにおける構造や機能の変化は、多くの神経変性疾患やCNS障害においてしばしば早期の病理変化となります4-7。初期のシナプス機能障害を検出するため、単一細胞での解像度をもち実験条件変化をリアルタイムで分析可能な生細胞画像診断が利用されています。本ニュースレターでは、CNS疾患や障害のin vitroやin vivo研究における生細胞画像診断の利用に関してお伝えします。
in vitroおよびin vivo生細胞イメージング実験をデザインする上で、適切なシナプス構造と機能(例えば、形態や電気的活性)をもつ健常かつ成熟したニューロンが必要です(図1)。一次イメージング標的は、早期に病態変化を受ける基質であるシナプス前やシナプス後の構造や関連タンパク質(例えば、シナプス小胞タンパク質、神経伝達物質受容体、イオンチャネル、足場タンパク質、および細胞骨格タンパク質[F-アクチン、微小管])です4(図1)。シナプス構造や機能の変化を評価する手法として、シナプス密度、神経突起長、スパイン密度、結節(神経突起が突出する細胞体上の部位)、樹状突起の分枝、および電気活性などを測定する方法が挙げられます4。
ヒト人工多能性幹細胞(hiPSC)由来ニューロンをはじめとするin vitro培養哺乳類ニューロンの生細胞イメージングは、生物学的関連性がより大きいと推定されるため利用されており8、これによりアルツハイマー病(AD)やパーキンソン病(PD)といったヒト神経変性疾患に関連する特有の力学的かつ機能的知見が明らかとなりました。アポリポタンパク質E(apoe-E)は、ADの病態形成に関与するタンパク質として知られていますが、apoe-Eやその代謝物はニューロンの生理に果たす役割は認識されていません。25kDa断片または全長apoEで慢性的に処理した分化型SH-SY5Y神経芽細胞腫細胞は、神経突起生成(生細胞イメージングで評価した神経突起長や細胞培養密度の陽性変化)を示します9。薬剤スクリーニングの予備試験でも、この手法で利益を得ることができます。ADでは最も一般的な薬物標的が2つあり、いずれもシナプスに対して早期病理学的効果があるタンパク質であるアミロイドβ(Aβ)とタウタンパク質です5-7。近年病理学的Aβに対するいくつかの候補抗体のスクリーニングにおいて、hiPSC由来ニューロンの生細胞イメージングが使用されました。ここでは、様々な抗体培養時間や濃度における神経突起長や樹状突起分岐点の変化を定量することによって陽性免疫療法の所見が評価されました10。
別のAβ研究として、Hongら11は、死後のADヒト脳抽出物より単離したAβオリゴマーで処理した生きたhiPSC由来ニューロンを画像化しました。彼らは、長期にわたる増強記録とともに神経突起長やシナプス可塑性の変化を定量することでオリゴマーの病態生理学を評価しました。タウタンパク質は、タウ立体構造に感受性をもつ最初の遺伝的にコードされたフェルスター共鳴エネルギー転位(FRET)センサー構築を含む新規技術の的となっています。このセンサーは、生きたHeLa細胞や不死化HT22海馬ニューロンにおいて、薬理学的治療後に微小管(MTs)存在下または非存在下で野生型および病理学的変異体のタウタンパク質の立体構造をモニターします12。このタウFRETセンサーでは、MTsへのタウ結合調節、可溶性と不溶性(病理学的)タウの比率、および非病理学的形態を支持するタウ立体構造にどのように影響するかに関する貴重な定量的かつ定性的なデータを提供します。
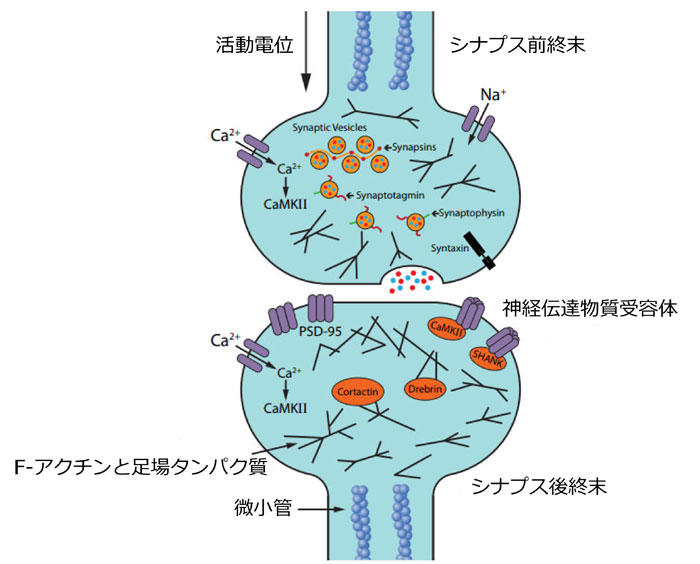
図1. ニューロン、シナプス、シナプス活性、およびシナプス可塑性の生細胞画像診断における分子および細胞標的。
in vitro細胞培養モデルに対して、in vivo動物モデルがあります。動物全身におけるニューロンの生細胞イメージングは、しばしば二光子顕微鏡法により行われます。この方法では、相互接続されたサポートネットワークのより大きな設定内において、機能性ニューロンを自然の状態で、単一細胞解像度において観察することができます13。このように、動物における生細胞イメージングは、可視化し動的な細胞プロセスをリアルタイムで分析することができます。さらに、単一細胞in vivo画像化により、感覚入力、行動、および薬物治療に伴うニューロンの機能性応答を定量化できます13。in vivo二光子生細胞イメージングは、α-シヌクレインを標的する抗-PD薬の作用機序の探索14や、死滅または死にゆくニューロンと置換する目的で損傷生体脳領域へ胚細胞移植を行うことの実現可能性、適切なタイミング、宿主、およびドナー条件の評価15-17に利用されています。さらに、in vivoイメージングにより新しい治療アプローチが明らかにできます。PDのMPTPマウスモデルでは、生細胞イメージングにより、MPTP処理マウスにおいて皮質運動ニューロンの構造的かつ機能的シナプス可塑性がドーパミン作動性ニューロンの選択的欠損により影響を受けることが示されています。これより、運動皮質の特定領域におけるニューロン活性を調節が、PD18に関連する運動機能障害の治療となり得る可能性が示唆されます。
まとめ
生細胞イメージングは、基礎的な疾患/障害生物学だけでなく薬理学的、遺伝学的、および、行動療法介入の機能的結果についてリアルタイムで洞察を得ることができるため、CNS疾患や障害の研究において非常に有用なツールです。超解像顕微鏡や自動化生細胞イメージングの進歩と合わせると19、初期の治療的介入により停止したり回復したりできるかもしれない最初の病理学的シナプス変化に焦点をあてる比類のない機会となります。Cytoskeleton 社では、F-アクチン、微小管、DNA、およびリソソームに対する生細胞イメージング用プローブや、精製済み細胞骨格タンパク質、活性化アッセイキット、および抗体もご用意しています。
参考文献
- Neurological disease models made clear. Nat. Med. (Editorial, published September 2015). 21, 964.
- Schlachetzki J.C. et al. 2013. Studying neurodegenerative diseases in culture models. Rev. Bras. Psiquiatr. 35, S92-100.
- Hughes P. et al. 2018. The costs of using unauthenticated, over-passaged cell lines: how much more data do we need. Biotechniques. 43, 575, 577-578, 581-582
- Verstraelen P. et al. 2018. Image-based profiling of synaptic connectivity in primary neuronal cell culture. Front. Neurosci. 12, 389.
- Hoover B.R. et al. 2010. Tau mislocalization to dendritic spines mediates synaptic dysfunction independently of neurodegeneration. Neuron. 68, 1067-1081
- Spires-Jones T.L. and Hyman B.T. 2014. The intersection of amyloid beta and tau at synapses in Alzheimer’s disease. Neuron. 82, 756-771.
- Bayer T.A. and Wirths O. 2010. Intracellular accumulation of amyloid-beta - a predictor for synaptic dysfunction and neuron loss in Alzheimer’s disease. Front. Aging Neurosci. 2, 8
- Unternaehrer J.J. and Daley G.Q. 2011. Induced pluripotent stem cells for modelling human diseases. Phil. Trans. R. Soc. B. 366, 2274-2285.
- Munoz S.S. et al. 2018. The serine protease HtrA1 contributes to the formation of an extracellular 25-kDa apolipoprotein E fragment that stimulates neuritogenesis. J. Biol. Chem. 293, 4071-4084
- Jin M. et al. 2018. An in vitro paradigm to assess potential anti-Aβ antibodies for Alzheimer’s disease. Nat. Commun. 9, 2676.
- Hong W. et al. 2018. Diffusible, highly bioactive oligomers represent a critical minority of soluble Aβ in Alzheimer’s disease brain. Acta Neuropathol. 136, 10-40
- Di Primio C. et al. 2017. The distance between N and C termini of tau and of FTDP-17 mutants is modulated by microtubule interactions in living cells. Front. Neurosci. 10, 210.
- White M.D. et al. 2018. In vivo imaging of single mammalian cells in development and disease. Trends Mol. Med. 24, 278-293.
- Wrasidlo W. et al. 2016. A de novo compound targeting alpha-synuclein improves deficits in models of Parkinson’s disease. Brain. 139, 3217-3236.
- Falkner S. et al. 2016. Transplanted embryonic neurons integrate into adult neocortical circuits. Nature. 539, 248-253.
- Peron S. et al. 2017. A delay between motor cortex lesions and neuronal transplantation enhances graft integration and improves repair and recovery. J. Neurosci. 37, 1820-1834.
- Wang C. et al. 2016. Infiltrating cells from host brain restore the microglial population in grafted cortical tissue. Sci. Rep. 6, 33080.
- Guo L. et al. 2015. Dynamic rewiring of neural circuits in the motor cortex in mouse models of Parkinson’s disease. Nat. Neurosci. 18, 1299-1309.
- Shin H.Y. et al. 2018. Using automated live cell imaging to reveal early changes during human motor neuron degeneration. eNeuro. doi: 10.1523/ENEURO.0001-18.2018.
Live Cell Imaging Products
[商品詳細]
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
SiR-Actin Kit |
CYT | CY-SC001 | 1 KIT [50-300 slides] |
¥182,000 |
SiR-Tubulin Kit |
CYT | CY-SC002 | 1 KIT [50-300 slides] |
¥182,000 |
Cytoskeleton Kit (SiR-Actin + SiR-Tubulin) |
CYT | CY-SC006 | 1 KIT [50-300 slides] |
販売終了 |
SiR-DNA Kit |
CYT | CY-SC007 | 1 KIT [50-300 slides] |
¥120,000 |
SiR-Lysosome Kit |
CYT | CY-SC012 | 1 KIT [50-300 slides] |
¥131,000 |
SiR700-Actin Kit |
CYT | CY-SC013 | 1 KIT [35-200 slides] |
¥182,000 |
SiR700-Tubulin Kit |
CYT | CY-SC014 | 1 KIT [35-200 slides] |
¥182,000 |
SiR700-DNA Kit |
CYT | CY-SC015 | 1 KIT [35-200 slides] |
¥120,000 |
SiR700-Lysosome Kit |
CYT | CY-SC016 | 1 KIT [35-200 slides] |
¥131,000 |
G-LISA Activation Assay Kits
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
RhoA G-LISA(R) Activation Assay (absorbance) |
CYT | BK124 | 96 ASSAY |
CYT社 BK124L 1 を参照 |
RhoA G-LISA GTPase Activation Assay (Luminescence format) |
CYT | BK121 | 96 ASSAY |
¥317,000 |
Actin Biochem Kits
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Actin Binding Protein Spin-Down Assay Biochem Kit, Rabbit |
CYT | BK001 | 1 KIT [30-100 assays] |
¥268,000 |
Actin Binding Protein Spin-Down Assay Biochem Kit, Human |
CYT | BK013 | 1 KIT [30-100 assays] |
¥272,000 |
Actin Polymerization Biochem Kit (fluorescence format), Rabbit |
CYT | BK003 | 1 KIT [30-100 assays] |
¥304,000 |
G-Actin/F-actin In Vivo Assay Biochem Kit, Mouse |
CYT | BK037 | 1 KIT [30-100 assays] |
¥264,000 |
Tubulin Biochem Kits
[商品詳細]
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Tubulin polymerization assay using >99% pure tubulin - OD based, Porcine |
CYT | BK006P | 1 KIT [24 assays] |
¥300,000 |
Tubulin polymerization assay using >99% pure tubulin - fluorescence based |
CYT | BK011P | 1 KIT [96 assays] |
¥317,000 |
Microtubule Binding Protein Spin-Down Assay Biochem Kit |
CYT | BK029 | 1 KIT [30-100 assays] |
¥265,000 |
Microtubule/Tubulin In Vivo Assay Biochem Kit |
CYT | BK038 | 1 KIT [30-100 assays] |
販売終了 |
■ CYTOSKELETON NEWS バックナンバー
- 2020年10月号 紡錘体 - 可視化に向けた新規ツール
- 2020年8月号 細胞膜染色用蛍光プローブ
- 2020年4月号 生細胞におけるF-アクチンプローブ
- 2020年3月号 コロナウイルスと細胞骨格
- 2020年2月号 タウ(Tau)の将来性をMapping
- 2020年1月号 Rho GTPaseによる細胞遊走制御
- 2019年12月号 表現型プロファイリング:アクチンに焦点を当てたがん治療
- 2019年11月号 チューブリンの過剰グルタミル化、ミトコンドリア、神経変性
- 2019年9月号 細胞運動性を制御するために相互作用する膜張力とアクチン細胞骨格
- 2019年8月号 Rac1B、がん、およびRac1
- 2019年7月号 Rhoファミリー GTPases、神経可塑性、およびうつ状態
- 2019年6月号 アクチンメチオニン酸化: 動的制御の次の段階
- 2019年5月号 ミクログリアと神経変性疾患
- 2019年2月号 生細胞画像化に対するCNS疾患や障害
2018年
- 2018年12月号 アクチン細胞骨格とメカノトランスダクション(機械的シグナル伝達)
- 2018年11月号 軸索再生と細胞骨格
- 2018年10月号 ニューロンにおける微小管と極性
- 2018年8月号 Rab GTPase と 神経変性
- 2018年7月号 SUMO レスリング: バランスが全て
- 2018年6月号 なぜ K-Ras は発がん特異性を示すのか?
- 2018年5月号 治療標的としてのユビキチンプロテアソームシステム:チューブリンは関与するか?
- 2018年4月号 RhoファミリーGEFと樹状突起スパインの構造的可塑性
- 2018年3月号 βカテニンとTFC/LEF-1の翻訳後修飾による標準的なWntシグナル制御
- 2018年2月号 がん抑制遺伝子p53の翻訳後修飾による機能の調整
- 2018年1月号 自閉スペクトラム症におけるGEF Trioの役割
2017年
- 2017年12月号 プロフィリン: アクチン結合タンパク質の多機能な役割
- 2017年11月号 ミトコンドリアにおけるアセチル化:新たな考え方と治療への応用の可能性
- 2017年9月号 翻訳後修飾のアセチル化による微小管の安定化
- 2017年8月号 神経軸索におけるアクチンリングを基盤とした周期的膜骨格(PMS)
- 2017年7月号 E3ユビキチンリガーゼMdm2によるがん抑制遺伝子p53の翻訳後制御
- 2017年6月号 多能性幹細胞(PSC)での転写因子による翻訳後制御
- 2017年5月号 Arf6 GEF と癌細胞の浸潤・転移
- 2017年4月号 PTEN(Phosphatase and Tensin Homolog)による翻訳後制御
- 2017年3月号 Tau の翻訳後修飾: アルツハイマー病の治療標的
- 2017年2月号 樹状細胞の移動におけるアクチン結合タンパク質とF-アクチン
2016年
- 2016年11月/12月号 GEF を介した GTPase シグナル伝達の低分子阻害剤
- 2016年9月号 FtsZ タンパク質: 抗菌薬の新規ターゲット
- 2016年7月号 翻訳後修飾(PTM)は心臓病において細胞骨格タンパク質を調節する
- 2016年6月号 モータータンパク質キネシンと神経変性
- 2016年5月号 チロシンリン酸化は Rhoファミリー GTPase 活性を調節する
- 2016年4月号 Rac1と糖尿病: ポジティブな役割とネガティブな役割
- 2016年3月号 SUMO化: 細胞骨格タンパク質の機能を調節するレギュレーター
- 2016年1月/2月号 ビメンチン中間径フィラメント: リン酸化による調節
2015年
- 2015年8月号 タンパク質調節に不可欠な翻訳後修飾
- 2015年7月号 アクチン細胞骨格のライブセルイメージング
- 2015年6月号 有糸分裂に関わるタンパク質のSUMO化: 局在と機能
- 2015年5月号 Ras 癌の治療: 5つの有望なターゲット
- 2015年4月号 Ras 依存性の癌で注目される YAP1
- 2015年3月号 増刊号 統合失調症において遺伝子変異により誘導されるアクチン依存のシナプスの変化
- 2015年3月号 Ral GTPase を調節する翻訳後修飾
- 2015年1月/2月号 RhoA のリン酸化はシグナル伝達を調節する
- 2015年1月号 増刊号 微小管を不安定化する suprafenacine: 新規抗癌剤のリード化合物としての可能性
2014年
- 2014年12月号 増刊号 RhoA は心筋細胞におけるアクチン細胞骨格の再構成とグルコース取り込みを仲介する
- 2014年11月号 増刊号 樹状突起の形態形成: ドーパミンD1受容体 および Rho ファミリー GTPase による制御
- 2014年11月/12月号 GTPase 活性化アッセイ: アイソフォームの検出
- 2014年10月号 アルギニンの正電荷を消失させるシトルリン化
- 2014年9月号 キネシンサブドメインの探索
- 2014年9月号 増刊号 アクチン結合タンパク質コフィリンの S-ニトロシル化: 細胞移動に対する影響
- 2014年8月号 増刊号 原発性硬化性胆管炎における N-Ras 発現および活性
- 2014年8月号 SUMO化: 細胞骨格タンパク質を標的とした翻訳後修飾
- 2014年7月号 Sos/K-Ras 結合を介して Ras シグナル伝達を制御する新しい低分子阻害剤
- 2014年6月号 増刊号 頭頸部扁平上皮癌における microRNA-138 による RhoC のダウンレギュレーション
- 2014年6月号 Rho GTPase と活性酸素種: クロストークとフィードバック
- 2014年5月号 ミオシンのアセチル化はサルコメアの構造と機能を調節する
- 2014年4月号 リジンのアセチル化 - 多様な細胞プロセスの制御因子
- 2014年3月号 インテグリンを介したβ-アクチンの酸化還元制御: PDIの出現
- 2014年1/2月号 ダイニン: 一つのモーターが関わる複数の神経変性疾患
2013年
- 2013年11/12月号 ダイニン:チームとして強力に作用するモータータンパク質
- 2013年10月号 神経変性:Rhes、SUMO化、ハンチントン病
- 2013年9月号 モノユビキチン化:タンパク質調節のダイナミックなタグ
- 2013年8月号 Ras及びRhoのプレニル化による翻訳後修飾:癌創薬における役割
- 2013年7月号 アクチンが引き起こす膜突起による浸潤:コルタクチン
- 2013年6月号 アクチン修飾と細胞骨格
- 2013年5月号 微小管内部の実体
- 2013年4月号 神経変性におけるTauの多面性
- 2013年3月号 蛍光フィブロネクチンタンパク質を用いた特発性肺線維症の創薬
- 2013年1/2月号 樹状突起棘:発生におけるArf6の役割
2012年
- 2012年11/12月号 ミオシンの小分子モジュレーター
- 2012年10月号 Rhoファミリーパスウェイのユビキチン化と制御
- 2012年9月号 神経変性におけるRac1 GTPaseの機能
- 2012年8月号 上皮間葉転換(EMT)とRhoファミリー低分子量G-タンパク質の関与
- 2012年7月号 チューブリンの多重修飾:グルタミル化とグリシル化
- 2012年6月号 細胞接着のフィブロネクチン制御と原線維形成
- 2012年5月号 アクチン酸化サイクルの機能
- 2012年4月号 トラフィッキング:ArfとCdc42/Racの結合
- 2012年3月号 G-LISAを用いた心臓研究: 糖尿病性心筋症におけるRho経路に関する研究
- 2012年1月/2月号 FtsZ: 新たな抗生剤の標的となるチュ−ブリンホモログ
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について























 このページを印刷する
このページを印刷する














