記事ID : 15159
Ras 癌の治療: 5つの有望なターゲット CYTOSKELETON NEWS 2015年5月号

Ras 癌の治療: 5つの有望なターゲット
Ras GTPアーゼは、癌の形態ならびに正常な細胞増殖や分化に関わる複数のシグナル伝達経路において重要な役割を果たしています1,2。Ras の3種類のアイソフォームである H-Ras、N-Ras、K-Ras は、ヒト腫瘍において発癌作用を示す遺伝子として、30年以上前に同定されました1,2。Ras シグナル伝達の異常は、ヒト癌の 30% 以上(一般的には肺癌、大腸癌、膵臓癌)で同定されています1,3。特に K-Ras は、癌研究において最も重要な Ras タンパク質であると考えられており、21% 以上のヒト癌に関与しています4。広範な研究がなされているにも関わらず、効果的な Ras 阻害剤が同定されていないことから、K-Ras をターゲットとした新薬の開発は非常に困難であると考えられています。これまではほとんど成功例がありませんが、近年の研究の進歩により、Ras タンパク質を直接阻害する治療薬だけではなく、GEF、GAP、下流のタンパク質、翻訳後修飾などを標的とする間接的な阻害剤の開発が期待されています(図1)。本稿では、Ras 癌治療における有望な5つのターゲットに注目します。
1. 変異型 K-Ras を直接ターゲットにする
K-Ras の変異型と野生型の選択は、変異がエフェクター結合部位から離れているため、困難であることが示されています1。近年発見された K-Ras 変異体(G12C: 12番目のグリシンがシステインに変異)のアロステリック switch II ポケット(S-IIP)は、K-Ras を阻害するための新しいターゲットとなる可能性があります5。この報告から間もなく、システイン変異に結合してSOSを介したヌクレオチド交換を阻害することにより、K-Ras 変異体を阻害する低分子化合物が開発され、低分子化合物を介して K-Ras を直接ターゲットにする治療が期待されています5。SOS および Ras の阻害に関しては、CYTOSKELETON NEWS 2014年7月号「Sos/K-Ras 結合を介して Ras シグナル伝達を制御する新しい低分子阻害剤」に詳しくまとめています。
2. GEF および GAP をターゲットにする
哺乳類の発現する3種類の GEF である SOS、RasGRF、RasGRP は、一般的に Ras の活性化因子であると考えられています6。GEF は Ras の活性化を仲介するにも関わらず、癌において GEF の変異が見つかることは非常にまれです。一方、GAP(NF1、p120GAP/RASA1、SynGAP/RASA5、GAP1 ファミリー、DAB2IP、GAPVD1など)は、Ras が関連する癌の数種類に関与します6,7,8 (図1)。腫瘍形成における GEF/GAP の役割については、Anne Hennig 博士らによる総説に詳しくまとめられています6。
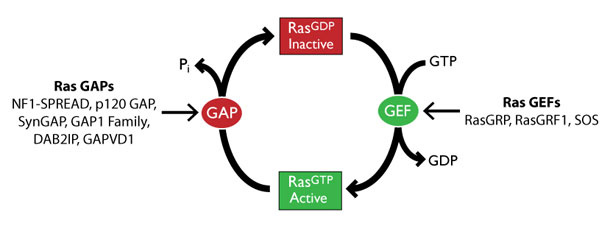
図1 Ras 活性化に関与する GAP および GEF を示した Ras GTPase サイクルの概略図
3. 下流のタンパク質をターゲットにする
MAP キナーゼ(MAPK)キナーゼ(MEK)は、Ras 活性化の下流で起こる MAPK 経路のタンパク質です。FDA 承認薬トラメチニブ(Mekinist™)のターゲットであり、患者数人に対して臨床上有効であることが示されています9。しかし、重篤な副作用を起こさずに、有効血中薬物濃度を維持することは困難です9。Ras 活性化の下流にあるもう一つの経路は Merlin/Hippo プロテインキナーゼ経路で、増殖を促進する転写コアクチベーターである YAP の活性を調節します。この経路が活性化されると、細胞増殖を制限してアポトーシスを促進し、Ras 依存性の癌に重要な役割を果たします10-12。Merlin は Hippo 経路を調節し、Merlin の減少は Hippo 経路の不活性化につながります10。Merlin は膜および核に局在することが報告されていますが、腫瘍抑制部位については未解明なままです。しかし、近年の報告により、Merlin は細胞膜で Hippo 経路を介した腫瘍形成を抑制するのではなく、核内で E3 ユビキチンリガーゼ複合体 CRL4DCAF1 と Hippo 経路の構成因子であるセリン/スレオニンキナーゼ LATS1/2 との相互作用を阻害することによって作用することが示唆されます13。核に局在する Merlin は CRL4DCAF1 と相互作用して、LATS キナーゼによる CRL4DCAF1 のユビキチン化を阻害します。その後、 CRL4DCAF1 は、YAP をリン酸化することで不活性化し、細胞質への蓄積を引き起こします10。しかし、YAP が活性化される(非リン酸化)と、Merlin は転写因子 TEAD と共に変異型および野生型 Ras タンパク質の発現を増加させます10,13。YAP1と Hippo 経路については、CYTOSKELETON NEWS 2015年4月号に詳しくまとめています。
4. 翻訳後修飾をターゲットにする
Ras タンパク質は、RCE1によるタンパク質切断、ファルネシル化、ICMT によるカルボキシメチル化、パルミトイル化など、数種類の翻訳後修飾を受けます14。近年、さらにモノユビキチン化やアセチル化などの翻訳後修飾が、Ras 活性化の調節に重要な役割を果たすことが示されています。K-Ras の Lys147 がモノユビキチン化されると、GTP との結合を促進します15。K-Ras の Lys104 がアセチル化されると、GEF によるヌクレオチド交換活性が低下することから、 SIRT2 および HDAC6 脱アセチル化酵素は、Ras を阻害するためのターゲットとなることが示唆されます16。
5. ナノ医療と siRNA によるノックダウン
近年、膵臓癌の治療として、変異型 K-Ras をターゲットに siRNA および ヒ素を内包したベシクルを同時にデリバリーすると、アポトーシスを誘発し、変異型 K-Ras の増殖・転移能を下方制御することが報告されました17。 また、K-Ras と RAF および PI3K との結合を阻害することをターゲットとした siRNA 治療は、異種移植モデルにおいて K-Ras 変異大腸癌に有効であることが示されています18。
まとめ
さらに Ras 調節メカニズムを研究するために、高感度かつ定量的に Ras の活性化レベルを測定する方法が重要になります。Cytoskeleton社では、低分子量Gタンパク質の活性化レベルの測定に広く使用できる pull-down アッセイや G-LISA 活性アッセイなど、癌治療の研究に有用なツールを多数ご提供しております。Ras 活性化経路を解明するために、低分子量Gタンパク質抗体、活性化因子、阻害物質などをご利用いただけます。
参考文献
- Wang W. et al. 2012. Ras inhibition via direct Ras binding—is there a path forward. Bioorg. Med. Chem. Lett. 22, 5766-5776.
- Castellano E. and Santos E. 2011. Functional specificity of Ras isoform: so similar but so different. Genes Cancer. 2, 216-231.
- Burns M.C. et al. 2014. Approach for targeting Ras with small molecules that activate SOS-mediated nucleotide exchange. Proc. Natl. Acad. Sci. U.S.A. 111, 3401-3406.
- Baines A. et al. 2011. Inhibition of Ras for cancer treatment: the search continues. Future Med. Chem. 3, 1787-1808.
- Ostrem J. et al. 2013. K-Ras (G12C) inhibitors allosterically control GTP affinity and effector interactions. Nature. 503, 548-551.
- Hennig A. et al. 2015. Ras activation revisited: role of GEF and GAP systems. Biol. Chem. doi: 10.1515/hsz-2014-0257.
- Nissan M.H. et al. 2014. Loss of NF1 in Cutaneous Melenama Is Associated with RAS Activation and MEK Dependence. Cancer Res. 74, 2340
- Stephen A.G. et al. 2014. Dragging Ras Back in the Ring. Cancer Cell. 25, 272-281.
- Online: http://www.cancer.gov/cancertopics/research-updates/2013/MEK.

- Online: http://www.cancer.gov/researchandfunding/priorities/ras/advance-research/events/ras-fagin-video.Hong X. et al. 2014.
- Opposing activities of the Ras and Hippo pathways converge on regulation of YAP protein turnover. EMBO J. 33, 2447-2457.
- Kapoor A. et al. 2014. Yap1 activation enables bypass of oncogenic Kras addiction in pancreatic cancer. Cell. 158, 185-197.
- Li W. et al. 2014. Merlin/NF2 loss-driven tumorigenesis linked to CRL4(DCAF1)-mediated inhibition of the hippo pathway kinases Lats1 and 2 in the nucleus. Cancer Cell. 26, 48-60.
- Gysin S. et al. 2011. Therapeutic strategies for targeting ras proteins. Genes Cancer. 2, 359-372.
- Sasaki A.T. et al. 2011. Ubiquitination of K-Ras enhances activation and facilitates binding to select downstream effectors. Sci. Signal. 4, ra13.
- Yang M.H. 2013. HDAC6 and SIRT2 Regulate the acetylation state and oncogenic activity of mutant K-RAS. Mol. Cancer Res. 11, 1072-1077.
- Zeng L. et al. 2014. Combination of siRNA-directed Kras oncogene silencing and arsenic-induced apoptosis using a nanomedicine strategy for the effective treatment of pancreatic cancer. Nanomedicine. 10, 463-472.
- Yuan T.L. et al. 2014. Development of siRNA Payloads to Target KRAS-Mutant Cancer. Cancer Discovery. 4, 1182.
アセチルリジン マウスモノクローナル抗体
- アセチルリジン マウスモノクローナル抗体
- 翻訳後修飾されたアセチル化リジンを幅広く検出
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Anti Acetyl Lysine (Trial size), (Mouse) , 3C6.08.20 |
CYT | AAC01-S | 25 UL [1 x 25 μl] |
¥38,000 |
Anti Acetyl Lysine, (Mouse) , 3C6.08.20 |
CYT | AAC01 | 200 UL [2 x 100 μl] |
CYT社 AAC01L 2*100 を参照 |
ホスホチロシン(リン酸化チロシン) マウスモノクローナル抗体
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Anti Phosphotyrosine (Trial size), (Mouse) , 27B10 |
CYT | APY03-S | 1*25 UL |
¥18,000 |
Anti Phosphotyrosine, (Mouse) , 27B10.4 |
CYT | APY03 | 2*100 UL |
CYT社 APY03 3*100 を参照 |
SUMO-2/3 マウスモノクローナル抗体(クローン 12F3)
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Anti SUMO-2/3 (Trial size), (Mouse) , 12F3 |
CYT | ASM23-S | 25 UL [1 x 25 μl] |
¥38,000 |
Anti SUMO-2/3, (Mouse) , 12F3 |
CYT | ASM23 | 200 UL [2 x 100 μl] |
CYT社 ASM23L 2*100 を参照 |
ユビキチン マウスモノクローナル抗体
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Anti Ubiquitin (Trial size), (Mouse) , P4D2 |
CYT | AUB01-S | 1*25 UL |
¥38,000 |
Anti Ubiquitin, (Mouse) , P4D2 |
CYT | AUB01 | 2*100 UL |
CYT社 AUB01L 2*100 を参照 |
Ras G-LISA® 活性型低分子量Gタンパク質定量キット
- G-LISA® 活性型低分子量Gタンパク質定量キット
- 少量のサンプルから、3時間以内で活性型低分子量Gタンパク質を測定するキット
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Ras G-LISA GTPase Activation Assay Kit (Colorimetric Based) |
CYT | BK131 | 1 KIT [96 assays] |
¥317,000 |
Ras プルダウンアッセイ Biochem Kit™
- 活性型低分子量Gタンパク質 プルダウンアッセイ Biochem Kit™
- 低分子量Gタンパク質活性化を、プルダウンアッセイで簡単に検出!
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
Ras Activation Assay Biochem Kit |
CYT | BK008 | 1 KIT [50 assays] |
CYT社 BK008L 1 を参照 |
RhoGEF Exchange アッセイ Biochem Kit™
- RhoGEF exchange アッセイキット
- GTPase(GTPアーゼ)のヌクレオチド交換を蛍光により測定
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
RhoGEF exchange assay |
CYT | BK100 | 1 KIT [60-300 assays] |
¥240,000 |
SOS exchange ドメイン (564-1049) タンパク質
| 品名 | メーカー | 品番 | 包装 | 希望販売価格 |
|---|---|---|---|---|
SOS1 Ras GEF protein, Human |
CYT | CS-GE02 | 100 UG [1 x 100 μg] |
販売終了 |
SOS1 Ras GEF protein, Human |
CYT | CS-SOS1-B | 1 MG [1 x 1 mg] |
販売終了 |
■ CYTOSKELETON NEWS バックナンバー
- 2020年10月号 紡錘体 - 可視化に向けた新規ツール
- 2020年8月号 細胞膜染色用蛍光プローブ
- 2020年4月号 生細胞におけるF-アクチンプローブ
- 2020年3月号 コロナウイルスと細胞骨格
- 2020年2月号 タウ(Tau)の将来性をMapping
- 2020年1月号 Rho GTPaseによる細胞遊走制御
- 2019年12月号 表現型プロファイリング:アクチンに焦点を当てたがん治療
- 2019年11月号 チューブリンの過剰グルタミル化、ミトコンドリア、神経変性
- 2019年9月号 細胞運動性を制御するために相互作用する膜張力とアクチン細胞骨格
- 2019年8月号 Rac1B、がん、およびRac1
- 2019年7月号 Rhoファミリー GTPases、神経可塑性、およびうつ状態
- 2019年6月号 アクチンメチオニン酸化: 動的制御の次の段階
- 2019年5月号 ミクログリアと神経変性疾患
- 2019年2月号 生細胞画像化に対するCNS疾患や障害
2018年
- 2018年12月号 アクチン細胞骨格とメカノトランスダクション(機械的シグナル伝達)
- 2018年11月号 軸索再生と細胞骨格
- 2018年10月号 ニューロンにおける微小管と極性
- 2018年8月号 Rab GTPase と 神経変性
- 2018年7月号 SUMO レスリング: バランスが全て
- 2018年6月号 なぜ K-Ras は発がん特異性を示すのか?
- 2018年5月号 治療標的としてのユビキチンプロテアソームシステム:チューブリンは関与するか?
- 2018年4月号 RhoファミリーGEFと樹状突起スパインの構造的可塑性
- 2018年3月号 βカテニンとTFC/LEF-1の翻訳後修飾による標準的なWntシグナル制御
- 2018年2月号 がん抑制遺伝子p53の翻訳後修飾による機能の調整
- 2018年1月号 自閉スペクトラム症におけるGEF Trioの役割
2017年
- 2017年12月号 プロフィリン: アクチン結合タンパク質の多機能な役割
- 2017年11月号 ミトコンドリアにおけるアセチル化:新たな考え方と治療への応用の可能性
- 2017年9月号 翻訳後修飾のアセチル化による微小管の安定化
- 2017年8月号 神経軸索におけるアクチンリングを基盤とした周期的膜骨格(PMS)
- 2017年7月号 E3ユビキチンリガーゼMdm2によるがん抑制遺伝子p53の翻訳後制御
- 2017年6月号 多能性幹細胞(PSC)での転写因子による翻訳後制御
- 2017年5月号 Arf6 GEF と癌細胞の浸潤・転移
- 2017年4月号 PTEN(Phosphatase and Tensin Homolog)による翻訳後制御
- 2017年3月号 Tau の翻訳後修飾: アルツハイマー病の治療標的
- 2017年2月号 樹状細胞の移動におけるアクチン結合タンパク質とF-アクチン
2016年
- 2016年11月/12月号 GEF を介した GTPase シグナル伝達の低分子阻害剤
- 2016年9月号 FtsZ タンパク質: 抗菌薬の新規ターゲット
- 2016年7月号 翻訳後修飾(PTM)は心臓病において細胞骨格タンパク質を調節する
- 2016年6月号 モータータンパク質キネシンと神経変性
- 2016年5月号 チロシンリン酸化は Rhoファミリー GTPase 活性を調節する
- 2016年4月号 Rac1と糖尿病: ポジティブな役割とネガティブな役割
- 2016年3月号 SUMO化: 細胞骨格タンパク質の機能を調節するレギュレーター
- 2016年1月/2月号 ビメンチン中間径フィラメント: リン酸化による調節
2015年
- 2015年8月号 タンパク質調節に不可欠な翻訳後修飾
- 2015年7月号 アクチン細胞骨格のライブセルイメージング
- 2015年6月号 有糸分裂に関わるタンパク質のSUMO化: 局在と機能
- 2015年5月号 Ras 癌の治療: 5つの有望なターゲット
- 2015年4月号 Ras 依存性の癌で注目される YAP1
- 2015年3月号 増刊号 統合失調症において遺伝子変異により誘導されるアクチン依存のシナプスの変化
- 2015年3月号 Ral GTPase を調節する翻訳後修飾
- 2015年1月/2月号 RhoA のリン酸化はシグナル伝達を調節する
- 2015年1月号 増刊号 微小管を不安定化する suprafenacine: 新規抗癌剤のリード化合物としての可能性
2014年
- 2014年12月号 増刊号 RhoA は心筋細胞におけるアクチン細胞骨格の再構成とグルコース取り込みを仲介する
- 2014年11月号 増刊号 樹状突起の形態形成: ドーパミンD1受容体 および Rho ファミリー GTPase による制御
- 2014年11月/12月号 GTPase 活性化アッセイ: アイソフォームの検出
- 2014年10月号 アルギニンの正電荷を消失させるシトルリン化
- 2014年9月号 キネシンサブドメインの探索
- 2014年9月号 増刊号 アクチン結合タンパク質コフィリンの S-ニトロシル化: 細胞移動に対する影響
- 2014年8月号 増刊号 原発性硬化性胆管炎における N-Ras 発現および活性
- 2014年8月号 SUMO化: 細胞骨格タンパク質を標的とした翻訳後修飾
- 2014年7月号 Sos/K-Ras 結合を介して Ras シグナル伝達を制御する新しい低分子阻害剤
- 2014年6月号 増刊号 頭頸部扁平上皮癌における microRNA-138 による RhoC のダウンレギュレーション
- 2014年6月号 Rho GTPase と活性酸素種: クロストークとフィードバック
- 2014年5月号 ミオシンのアセチル化はサルコメアの構造と機能を調節する
- 2014年4月号 リジンのアセチル化 - 多様な細胞プロセスの制御因子
- 2014年3月号 インテグリンを介したβ-アクチンの酸化還元制御: PDIの出現
- 2014年1/2月号 ダイニン: 一つのモーターが関わる複数の神経変性疾患
2013年
- 2013年11/12月号 ダイニン:チームとして強力に作用するモータータンパク質
- 2013年10月号 神経変性:Rhes、SUMO化、ハンチントン病
- 2013年9月号 モノユビキチン化:タンパク質調節のダイナミックなタグ
- 2013年8月号 Ras及びRhoのプレニル化による翻訳後修飾:癌創薬における役割
- 2013年7月号 アクチンが引き起こす膜突起による浸潤:コルタクチン
- 2013年6月号 アクチン修飾と細胞骨格
- 2013年5月号 微小管内部の実体
- 2013年4月号 神経変性におけるTauの多面性
- 2013年3月号 蛍光フィブロネクチンタンパク質を用いた特発性肺線維症の創薬
- 2013年1/2月号 樹状突起棘:発生におけるArf6の役割
2012年
- 2012年11/12月号 ミオシンの小分子モジュレーター
- 2012年10月号 Rhoファミリーパスウェイのユビキチン化と制御
- 2012年9月号 神経変性におけるRac1 GTPaseの機能
- 2012年8月号 上皮間葉転換(EMT)とRhoファミリー低分子量G-タンパク質の関与
- 2012年7月号 チューブリンの多重修飾:グルタミル化とグリシル化
- 2012年6月号 細胞接着のフィブロネクチン制御と原線維形成
- 2012年5月号 アクチン酸化サイクルの機能
- 2012年4月号 トラフィッキング:ArfとCdc42/Racの結合
- 2012年3月号 G-LISAを用いた心臓研究: 糖尿病性心筋症におけるRho経路に関する研究
- 2012年1月/2月号 FtsZ: 新たな抗生剤の標的となるチュ−ブリンホモログ
商品は「研究用試薬」です。人や動物の医療用・臨床診断用・食品用としては使用しないように、十分ご注意ください。
※ 表示価格について























 このページを印刷する
このページを印刷する














